Хронический миелолейкоз у детей
Онкологическое заболевание такого типа не характерно для маленьких пациентов, частота установления диагноза составляет всего 1—5% клинических случаев всех детских лейкозов.
Данное патологическое состояние может протекать у маленького ребёнка по одному из двух типов:
- Ювенильный (относящийся к юношескому возрасту) хронический миелолейкоз. Эта разновидность болезни считается «взрослой» и преобладает у детишек после 5-т лет. Характерной особенностью такого типа заболевания является наличие в структуре лейкоцитов филадельфийской хромосомы.
- Инфантильный (недоразвитый, детский) миелоидный лейкоз. Этот тип заболевания поражает в основном малышей, не достигших двухлетнего возраста и отличается от ювенильной формы отсутствием в бластных клетках аномальной хромосомы. Ещё одной характерной особенностью этого типа заболевания является выраженное уменьшение у больных детей количества лейкоцитов в крови уже на ранней стадии развития патологического состояния, что приводит к частым кровотечениям, остановит которые очень сложно.
Стоит знать! Чем младше ребёнок, тем острее протекает у него заболевание. Чаще всего детская форма миелоидного лейкоза оказывается неизлечимой – смерть малыша наступает очень быстро из-за раннего развития тромбоцитопении, приводящей к обширным внутренним кровотечениям, остановить которые зачастую не представляется возможным.
Суть патологии
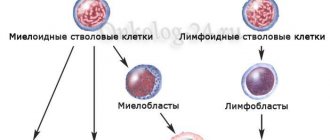
Хронический миелолейкоз (ХМЛ) характеризуется ростом содержания в крови гранулоцитов, одной из разновидностей лейкоцитов. Бесконтрольно формируясь в костном мозге, значительная их часть поступает в кровь незрелыми. Концентрация прочих видов лейкоцитов понижается, а молодые измененные клетки могут достигать зрелости.
В начале развития патологии количество лейкоцитов около 20000/мкл. При ее прогрессировании эта цифра изменяется до 400000/мкл. В крови обнаруживаются клетки разной степени зрелости – незрелые (промиелоциты, миелоциты, метамиелоциты) и зрелые (палочкоядерные нейтрофилы).
Фиксируются нарушения в хромосомах. Чаще всего заболевание провоцирует ощутимое возрастание концентрации прочих разновидностей лейкоцитов (базофилы и эозинофилы). Это свидетельство тяжелой формы ХМЛ. У пациентов увеличивается в размерах селезенка, в костном мозге и крови растет число миелобластов (прародители гранулоцитов).
Классификация хронического миелолейкоза
Хронический миелолейкоз в клинической практике принято подразделять на стадии в зависимости от того, насколько зрелыми являются клетки крови, входящие в состав опухолевых структур.
Читайте здесь: Лимфоузлы при раке крови
Развитие хронического миелолейкоза проходит через 3 фазы, для каждой из которых характерны определённые клинические признаки и морфологические изменения крови:
- Хроническая фаза или зарождение патологического процесса. Хронический миелолейкоз начинает развиваться постепенно. В первую очередь происходит миелоидная пролиферация (разрастание тканей костного мозга вследствие активации деления бластных клеток), что приводит к появлению в крови специфических изменений. Общие клинические признаки на этом этапе отсутствуют, поэтому хронический миелолейкоз в начале своего развития обычно бывает случайной находкой.
- Фаза акселерации, или переходная. На этой стадии клинические симптомы выражены слабо и состояние больных можно считать стабильным. Претерпевают изменение только гистологические признаки – начинается увеличение количественного состава лейкоцитов и миелоциты.
- Терминальная, завершающая фаза. Для окончательной стадии болезни характерно появление ярко выраженных клинических признаков, тяжело переносимых пациентами. Их появление указывает на начало бластного криза. Одной из особенностей заболевания, которой всегда сопровождается финальная фаза, является инфаркт селезенки и явное её увеличение за счёт накопления в органе кроветворения большого количества бластных клеток. Более чем у половины больных на этой фазе заболевания выявляют фиброз (увеличение тканей) костного мозга.
Стоит знать! Выявить хронический миелоидный лейкоз костного мозга, селезенки и крови обычно удаётся на последней фазе заболевания, что связано с отсутствием специфических симптомов на 1-й и 2-й стадии. Такое коварство болезни приводит к частым летальным исходам, но её медленное развитие, которое может продолжаться много лет, скрашивает эту картину, т. к. у многих больных удаётся выявить патологическое состояние в ранней фазе, при проведении диагностики по поводу другого заболевания.
Диагностика
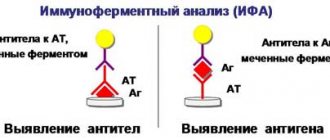
Для постановки диагноза проводится оценка имеющейся у пациента симптоматики и результатов лабораторных исследований крови. Общий анализ крови позволяет определить количество всех типов элементов. При хронической лейкемии выявляется повышенный уровень незрелых белых клеток и уменьшение количества тромбоцитов и эритроцитов. При проведении биохимического анализа выявляются признаки дисфункции селезенки и печени из-за проникновения в них раковых клеток.
Важная информация: Какие первые симптомы (признаки) лейкоза у детей до года и можно ли вылечить новорожденного ребенка от лейкемии
Для подтверждения диагноза часто назначается цитогенетический анализ, позволяющий исследовать хромосомный набор и выявить аномалию. Этот метод помогает точно определить тип лейкоза. Кроме того, нередко выполняются анализы гибридизации и полимеразной цепной реакции. Может проводиться биопсия костного мозга. К дополнительным исследованиям, применяющимся для оценки состояния внутренних органов, относятся КТ, МРТ и УЗИ.
Причины, провоцирующие развитие патологии крови
Хронический миелолейкоз – первое и единственное онкозаболевание, причина возникновения которого установлена достоверно. Основной предпосылкой, провоцирующей начало болезни, является появление в бластных клетках кроветворных органов аномальной хромосомы. Возникшее вследствие такой генетической мутации заболевание развивается очень медленно, и человек может прожить до престарелого возраста, так и не узнав о наличии в его крови онкологической патологии. Но развитие хронического миелолейкоза бывает и стремительным.
Читайте здесь: Лечение опухолей головного мозга
Быстро, за несколько месяцев, достигнуть финальной фазы болезнь может при наличии в жизни человека определённых факторов риска, основными из которых считаются:
- проживание в зонах с повышенным радиационным фоном или районах, находящихся в непосредственной близости от атомных электростанций;
- длительное лечение цитостатиками или бесконтрольный приём антибактериальных препаратов, имеющих повышенную токсичность;
- регулярное, продолжающееся длительное время, воздействие на организм человека токсических и химических веществ;
- наличие в анамнезе человека синдромов Клайнфелтера или Дауна.
Если в жизни человека присутствует хотя бы один из этих факторов риска, ему необходимо внимательнее относиться к своему самочувствию и при появлении минимальных нарушений в состоянии здоровья обратиться к специалисту за консультацией. Также людям, относящимся к группе риска рекомендована ежегодная профилактическая диагностика. Своевременное выявление патологического изменения состава крови позволяет полностью излечит развивающуюся хроническую форму миелолейкоза.
Причины развития болезни
Определенные гены контролируют рост и деление клеток. Одни стимулируют процесс развития (онкогены), другие замедляют его, вызывая физиологическую смерть клетки (супрессоры). Миелоидный лейкоз провоцируют мутации ДНК, способствующие распространению онкогенов или «отключению» супрессоров.
В клетках человеческого организма содержится по 23 пары хромосом. Обычно ХМЛ начинает развиваться при «обмене» фрагментов между 9 и 22 хромосомами (транслокация). Образуется аномальный ген, а 22 хромосома уменьшается в размерах. Трансформированная хромосома, названная филадельфийской, наблюдается в измененных клетках почти всех пациентов с диагнозом «хронический миелолейкоз». Именно она вызывает рост и хаотичное деление патологических клеток.
У незначительного числа больных вредоносные клетки измененной хромосомы не содержат. Считается, что у них пораженный ген образуется иначе. Крайне редко у пациентов не наблюдается ни измененного гена, ни «поломанной» хромосомы. Предполагается, что в этом случае развитие провоцируют неизвестные онкогены.
Дефект хромосомы специалисты не относят к генетическим, но исследования показали: велика вероятность развития патологии у детей, один из родителей которых имеет какие-либо генетические отклонения (синдром Дауна). На возникновение хронического миелоидного лейкоза влияют определенные внешние факторы:
- высокие дозы радиационного облучения;
- негативное воздействие химических веществ (спирты, эпоксидные смолы, алкены, кетоны, альдегиды);
- возраст (более 30 лет);
- пол (чаще заболевание диагностируют у мужчин).
Фактором риска может выступить ослабленный иммунитет. Курение способствует более тяжелому протеканию заболевания.
Симптомы онкопатологии кроветворных органов
Признаки недуга длительное время отсутствуют, первые специфические симптомы хронического миелолейкоза, заставляющие человека встревожится и посетить врача, появляются обычно в терминальной стадии болезни, когда вылечить её невозможно. Для начальной фазы заболевания характерны смазанные, носящие мягкий характер, симптомы. Но зная их, можно заподозрить развитие патологического состояния и, обратившись своевременно к гематоонкологу, диагностировать хронический миелолейкоз в ранней фазе, хорошо поддающейся терапии.
К основным признакам, которые должны вызывать тревогу, относятся:
- увеличение лимфатических узлов;
- анемия, характеризующаяся бледностью кожи;
- постоянное ощущение недомогания и усталости;
- необоснованная потеря аппетита и снижение веса;
- появление на кожных покровах синяков и кровоподтёков;
- частые и длительные наружные или внутренние кровотечения;
- ощущение переполненности левой стороны брюшной полости из-за увеличения размеров селезенки.
Эти симптомы типичны для многих заболеваний, но их появление нельзя игнорировать, т. к. они могут косвенно указывать на развивающуюся онкологию крови. Часто именно благодаря жалобам пациента на наличие у него этих признаков удаётся своевременно обнаружить опасное заболевание.
Виды терапии при хроническом миелолейкозе: медикаментозная, хирургическая, лучевая
Все лечебные мероприятия, применяемые для остановки онкологического процесса, поразившего кроветворные органы, назначаются гематоонкологом исходя из фазы развития заболевания, общих признаков, характеризующих его течение и выраженности сопровождающей хронический миелолейкоз клинической картины.
Терапевтические мероприятия назначаются индивидуально каждому пациенту, в зависимости от стадии протекания недуга:
- В начальной, хронической фазе особого лечения не требуется. Для поддержания у больных стабильного состояния им назначают общеукрепляющую терапию, заключающуюся в коррекции питания, снижении физической активности и соблюдении режима труда и отдыха.
- Фаза активизации хронического миелолейкоза требует расширения лечебных мероприятий. Больные в обязательном порядке проходят курсы биологической терапии Интерфероном и химии Хлорэтиламиноурацилом, Гексафосфамидом или Митобронитолом. По показаниям может быть назначена трансплантация костного мозга.
- При наступлении бластного криза лечение становится бесполезным. На этой заключительной фазе заболевания больным проводится исключительно симптоматическая терапия, позволяющая облегчить мучительные симптомы болезни и сохранить до последних дней качество жизни.
Виды миелоцитарного лейкоза
Различия по видам и формам заключаются в характере клинического течения и преобладающем типе накопившихся клеток.
По течению различают:
- острую форму;
- хронический миелоидный лейкоз.
При хроническом течении не только наблюдается замедленное развертывание симптомов болезни, но и в крови определяется особенный сдвиг, не характерный для острой формы. Поэтому в отличие от соматических заболеваний переход острой формы в хроническую невозможен.
Острый миелолейкоз, согласно классификации ВОЗ, подразделяется на виды в зависимости от выявленного воздействия разных участков хромосом.
Другая действующая классификация, утвержденная гематологами США, Франции и Великобритании, учитывает 9 подвидов по степени зрелости лейкоцитов. Выделение имеет смысл не только научный, но и предполагает одинаковую оптимальную стандартную терапию. К ним относят по степени дозревания клеток:
- лейкоз без созревания;
- с созреванием;
- с минимальной дифференцировкой клеточного состава.
По преобладающему составу клеточных форм:
- промиелоцитарный лейкоз;
- миеломоноцитарный — накопление клеток, предшественников моноцитов и гранулоцитов;
- миеломоноцитарный в сочетании с эозинофилией;
- миеломонобластный лейкоз — монобласты составляют большинство клонов;
- мегакариобластный;
- базофильный;
- группа эритроидных лейкозов.
Хронический миеломоноцитарный лейкоз тоже представляет собой несколько типов клеток-предшественников:
- миелоцитарный лейкоз с филадельфийской хромосомой и без нее;
- ювенильный миеломоноцитарный лейкоз;
- нейтрофильный и эозинофильный виды;
- первичный миелофиброз.
Прогнозы на выздоровление
Остановить развивающийся хронический миелолейкоз возможно только на начальной стадии патологического процесса при условии правильного проведения лечения. Но это случается очень редко, т. к. своевременное выявление заболевания представляет серьёзные сложности. Большая часть больных умирает в переходную или терминальную фазу хронического миелолейкоза. От диагностирования болезни и до наступления летального исхода на этих этапах болезни проходит около двух лет. Особую опасность представляет начало бластного криза – при этой фазе онкобольные живут не долее полугода. Самым неблагоприятным считается наличие в генах крови аномальной филадельфийской хромосомы.
Профилактика миелолейкоза
Определённых профилактических мероприятий, позволяющих предупредить хронический миелолейкоз, на сегодняшний день не существует. Единственное, что советуют гематоонкологи людям, находящимся в группе риска по развитию онкологического процесса в кроветворных органах, это регулярное прохождение скрининговых исследований.
К общим рекомендациям профилактики хронического миелолейкоза относятся:
- коррекция рациона питания с включением в ежедневное меню блюд, обогащённых витаминными и минеральными комплексами;
- полный отказ от пагубных пристрастий (курение, злоупотребление алкоголем, вечерние переедания), или сведение их к минимуму;
- ведение активного, здорового образа жизни с регулярными занятиями посильными видами спорта;
- уменьшение воздействия ультрафиолета: избегание пребывания под прямыми солнечными лучами.
Терапия патологии
Терапия хронического миелолейкоза определяется стадией патологии. На ранней стадии рекомендовано общеукрепляющее лечение, сбалансированное, обогащенное витаминами питание, регулярный диспансерный контроль. В остальных случаях при ХМЛ применяют медикаментозные средства, способствующие уменьшению величины селезенки и понижению активности злокачественных клеток. От адекватности и своевременности проводимой терапии напрямую зависит продолжительность жизни больного. Терапия осуществляется несколькими методами:
- Медикаментозное лечение (Цитозар, Альфа-интерферон, Миелосан);
- Трансплантация костного мозга (вероятность выздоровления выше при операции на ранних стадиях течения патологии, предпочтительные доноры – родственники пациента);
- Лучевая терапия (цель – уничтожение злокачественных клеток, сокращение темпов их развития);
- Удаление селезенки (обычно на последней стадии развития патологии). Показаниями к хирургическому вмешательству могут служить тромбоцитопения, угроза повреждения селезенки, явный дискомфорт, вызванный размерами органа.
Если прием лекарственных препаратов не дает ожидаемого эффекта, применяют лейкофорез – клеточное очищение крови от чрезмерного количества лейкоцитов. Иногда его применяют параллельно с медикаментозным лечением. На значительно увеличенную селезенку иногда воздействуют рентгеновскими лучами, это способствует уменьшению ее величины. При возникновении гнойных воспалительных очагов применяют антибиотики.
При развитии выраженной анемии, толерантной к цитостатикам, или при терапии железодефицитной анемии соответствующими препаратами железа показано переливание крови. Пациенты подлежат постановке на диспансерный учет, им необходимы регулярные осмотры и наблюдение за показателями крови. Самостоятельная терапия хронической формы миелоидного лейкоза несостоятельна и недопустима.
Прогрессирование патологии
При развитии патологии показаны цитостатики. Масштабность проводимого лечения зависит от фазы заболевания. Возникновение явных симптомов (увеличение органов, рост числа лейкоцитов в сравнении с более ранней стадией патологии) – повод для применения первично-сдерживающих подходов. Пациентам в небольших дозах амбулаторно прописывают гидроксимочевину – при условии контроля показателей крови. После ремиссии заболевания применяют поддерживающее лечение.
Развернутая стадия патологии
Если заболевание перешло в развернутую стадию, медикаментозное лечение проводят в зависимости от «группы риска» (гематологические показатели). При незначительных рисках изначально осуществляют лечение одним препаратом (монохимиотерапия), при высоком сразу рекомендуется применять несколько лекарственных средств одновременно (полихимиотерапия).
Завершив курс монохимиотерапии, сначала назначают то же средство, но в большей дозировке. При улучшении показателей крови его отменяют или снижают дозировку. Если применявшийся цитостатик не принес ожидаемого эффекта в течение месяца, осуществляют лечение другим лекарственным препаратом.
После курса химиотерапии проводят поддерживающее лечение (схема схожа со схемой первично-сдерживающей терапии). Используют лекарственные средства, оказавшиеся эффективными при курсовом лечении. Полихимиотерапию осуществляют при повышенной степени риска и на последней стадии ХМЛ. При бластном кризе терапия схожа с лечением острой лейкемии. Полихимиотерапию проводят короткими курсами по 5-14 дней. Продолжительность перерывов составляет 7-10 дней.
Альфа-интерферон
К принципиально новым средствам терапии хронического миелолейкоза относят альфа-интерферон – антагонист факторов роста. Он тормозит влияние мегакариоцитов на процесс кроветворения и препятствует размножению гранулоцитов. Помимо этого, альфа-интерферон активизирует противоопухолевый иммунитет, создавая условия для нормализации кроветворения.
Являясь цитостатиком, лекарственное средство не оказывает депрессивного воздействия на здоровые клетки. Лечение альфа-интерфероном может вызвать и цитогенетическую ремиссию – отсутствие филадельфийской хромосомы. Это говорит даже не о ремиссии, а о полном выздоровлении пациента.
Мер профилактики хронического миелолейкоза не существует. Возможно только предупреждение обострений патологии (поддерживающее лечение, предотвращение инсоляции, простудных болезней). Средняя продолжительность жизни при ХМЛ – три-пять лет, иногда – до восьми. После развития бластного криза больному редко удается прожить больше года.