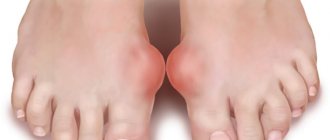
| Внутриутробные инфекции | |
| МКБ-10 | 35.-39. |
| МКБ-9 | 771 |
| MeSH | D018445 |
Внутриутробные инфекции
(ВУИ) — это различные инфекционные заболевания эмбриона, плода и новорождённого, заражение которыми происходит внутриутробно и в процессе родов[1]. Возбудителями инфекции могут быть вирусы, бактерии и (реже) паразиты. Путь передачи — вертикальный, от матери к плоду. Результатом инфицирования может стать выкидыш, врождённые пороки развития или острый инфекционный процесс у новорождённого.
Содержание
- 1 Эпидемиология 1.1 TORCH
- 2.1 Источник инфекции
- 6.1 Неонатальный герпес
Методы диагностики
Не существует никаких отличительных симптомов, позволяющих определить ВУИ без специальных исследований. Беременная женщина страдания плода не ощущает. Течение гестации не меняется, общее состояние будущей мамы не нарушается. Есть лишь некоторые косвенные признаки, позволяющие заподозрить инфицирование плода:
- Повышение тонуса матки. Матка пытается избавиться от зараженного плода, что может привести к выкидышу или преждевременным родам. Гипертонус миометрия ощущается как тянущие боли внизу живота и пояснице.
- Патологические вагинальные выделения говорят о наличии инфекции в половых путях, которая теоретически может попасть к плоду. Аномальными считаются выделения густые или слишком обильные, мутные, желтые и желто-зеленые, белые и сероватые с резким запахом. Сопровождаются зудом, жжением, болью во время интимной близости.
- Повышение температуры тела встречается при различных инфекционных заболеваниях, которые могут привести к заражению плода.
Для выявления ВУИ проводится обследование:
Лабораторные методы
В акушерской практике применяется:
- обзорный мазок на флору. Берется из влагалища, шейки матки и уретры;
- бактериологический посев из цервикального канала;
- полимеразная цепная реакция (ПЦР);
- иммунологические методы: ИФА и др.
Первые три метода позволяют выявить возбудителя, определить его тип и оценить чувствительность к лекарственным средствам. ИФА дает возможность обнаружить антитела к определенным микроорганизмам и оценить реакцию иммунной системы.
Важно! Указанные методы позволяют выявить только инфекцию матери, но не дают понять, проникли ли опасные микроорганизмы к плоду и как повлияли на его состояние.
Инструментальная неинвазивная диагностика
УЗИ – безопасный и достаточно эффективный метод, позволяющий заподозрить ВУИ. Оценка данных ультразвукового исследования проводится с учетом срока беременности.
В I триместре в пользу ВУИ говорят только косвенные факторы:
- повышение тонуса матки;
- признаки отслойки хориона;
- деформация плодного яйца;
- увеличение желточного мешка;
- недоразвитие хориона;
- несоответствие размеров эмбриона величине плодного яйца и др.
Во II и III триместрах о ВУИ говорит:
- изменение толщины плаценты;
- выявление взвеси в околоплодных водах;
- многоводие или маловодие;
- участки некроза головного мозга плода;
- выявление кальцинатов в печени и селезенке;
- водянка – скопление жидкости в мягких тканях;
- гипоксия плода;
- задержка развития плода.
Инструментальная инвазивная диагностика
Для выявления патологии применяются:
- биопсия хориона – забор материала для гистологического исследования;
- амниоцентез – оценка околоплодных вод;
- кордоцентез – забор пуповинной крови.
Внутриутробное инфицирование определяется при выделении возбудителя болезни или обнаружении антител YgM и YgG в пуповинной крови плода.
После рождения ребенка проводится гистологическое исследование плаценты. По определенным признакам можно подтвердить или опровергнуть внутриутробное инфицирование.
Эпидемиология
Истинная частота врождённых инфекций до настоящего времени не установлена, но, по данным ряда авторов, распространённость данной патологии в человеческой популяции может достигать 10 %.
Внутриутробным инфекциям присущи те же закономерности, что и инфекционным заболеваниям в целом.
Имеют ведущее место в структуре младенческой смертности.
Доля ВУИ в структуре перинатальной смертности в нашей стране составляет почти 25 %, вместе с тем трансплацентарное инфицирование плода считается одной из наиболее вероятных причин 80 % врождённых пороков развития, которые, в свою очередь, составляют около 30 % всех смертей детей до 1 года [2][3]
TORCH
В 1971 году ВОЗ выделил понятие TORCH — синдром
. Это аббревиатура наиболее часто встречающихся внутриутробных инфекций
Т — токсоплазмоз, О — другие, в которые входит микоплазма, сифилис, гепатиты, стрептококки, кандида и прочие вирусные и бактериальные инфекции, R — краснуха (rubella), C — цитомегаловирус, H — герпес
Если нет четкого этиологического диагноза, говорят о TORCH-синдроме.
ВИЧ-инфекция
Коварство ВИЧ-инфекции заключается в том, что латентный период ее может составлять срок до полутора лет. Если женщина подверглась инфицированию, то она может не знать об этом в момент планирования беременности, а современная медицина для благоприятного исхода беременности настаивает на предварительном медикаментозном лечении у ВИЧ-положительных матерей как минимум за 14 дней до зачатия. В случае обнаружения ВИЧ-инфекции у женщины после начала беременности пациентке назначают антибактериальные препараты, чтобы снизить содержание вируса в крови и уменьшить риск прохождения инфекции через плацентарный барьер. На ранних стадиях развития плода риск передачи болезни от матери к ребенку невелик, однако во время родов риск увеличивается. ВИЧ-инфекция увеличивает шансы преждевременных родов. Вероятность заражения плода в момент прохождения родового канала составляет 1:7. После рождения ребенок может инфицироваться при грудном вскармливании, поэтому ребенку назначают специальные детские смеси.
Последствия вынашивания ребенка матерью с положительной реакцией на ВИЧ с большой долей вероятности можно ожидать:
- Риски самопроизвольных выкидышей.
- Мертворождения.
- Гипотрофию.
- Поражения ЦНС.
- Хроническую диарею.
- Молочницу ротовой полости.
- Задержки развития.
Для профилактики внутриутробной инфекции ВИЧ-положительной женщине назначают антиретровирусную терапию, в которой используются диданозин и фосфазид, которыми заменяют обычно используемые зидовудин и невирапин. Эти препараты используются для предотвращения инфицирования плода на стадии вынашивания.
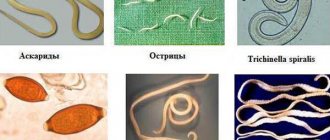
Этиология
Инфекционный процесс у плода могут вызывать самые разнообразные возбудители. Согласно этому принципу можно выделить несколько групп.
- Группа ВУИ, вызываемая вирусами: краснуха, ЦМВ, герпесвирусы, вирусный гепатит и др.
- Заболевания, вызываемые бактериями: сифилис, листериоз, туберкулёз, ЗППП
- Паразитарные инфекции: токсоплазмоз
- Грибковые инфекции, в том числе ятрогенного генеза
- Микст-инфекции (сочетанные).
Примечательно, что инфицирование этими же инфекциями в постнеонатальный период протекает в большинстве случаев бессимптомно или в виде лёгкого инфекционного процесса. Для плода особенно опасны возбудители инфекционных заболеваний, с которыми мать впервые встретилась во время беременности, так как в этот период первичный иммунный ответ снижен, тогда как вторичный — нормален.
Источник инфекции
Источником инфекции является мать. Но так же есть и ятрогенные причины инфицирования во время медицинских манипуляций[4][5].
Пути проникновения инфекции
- Трансплацентарный (гематогенный) путь — от матери к плоду через плаценту. Чаще передаются вирусные ВУИ, так как вирус легко проникает через гемато-плацентарный барьер (как и токсоплазма).
- Восходящий — когда инфекция из половых путей попадает в полость матки и затем может инфицировать плод. Чаще это бактериальные инфекции, ЗППП, хламидиоз, грибы, микоплазмы, энтерококки.
- Нисходящий путь — из маточных труб в полость матки
- Контактный (интранатальный) путь — заражение во время прохождения через родовые пути.
Исход инфицирования плода
- Инфекционное заболевание,
- Санация возбудителя с приобретением иммунитета,
- Носительство инфекционного агента с возможностью развития заболевания в будущем. Таким образом, наличие инфекции у матери, инфекционного поражения последа и инфицирование не означают 100 % развитие ВУИ у плода и новорождённого[1]
Лечение внутриутробных инфекций
Надо сказать, что не для всех внутриутробных инфекций можно подобрать лечение. Иногда вылечить их невозможно. Для подобной терапии прежде всего необходимо установить состояние матери и ребенка и лишь потом назначать соответствущее лечение. Лечение при помощи антибиотиков показано лишь в особо опасных случаях. Также оно подбирается в зависимости от возбудителя инфекции. Иногда бывает достаточно назначения женщине иммуноглобулинов для поддержания иммунной системы повышения иммунного противостояния возбудителю.
В некоторых случаях делают вакцинацию уже при течении беременности. Например, могут поставить вакцину против герпеса. Помимо этого, на способы лечения оказывает влияние и срок беременности.
И, надо отметить, что лучшее, что может сделать будущая мама — это не допустить развития внутриутробной инфекции, что поможет избежать дальнейших проблем и патологий. ПОэтому лучше всего соблюдать в отношении этого профилактические меры. К профилактическим мерам относится прежде всего — планирование беременности.
На этапе планирования женщина может сдать все необходимые анализы, проверить здоровья и устранить проблемы, если они имеются. При планировании пройти обследование необходимо обоим партнерам и если какие-то заболевания выявлены у мужчины, ему тоже необходимо провести необходимое лечение.
Помимо этого, уже во время беременности женщине необходимо тщательно следить за своей гигиеной, мыть рук, овощи и фрукты, а также гигиена нужна в отношениях с половым партнером.
Правильное питание укрепляет защитные силы организма и благотворно влияет на здоровье женщины, а значит тоже является хорошей профилактикой в отношении всевозможных инфекционных заболеваний.
Во время беременности женщина должна особенно внимательно следить за своим здоровьем, своевременно сдавать необходимые анализы и проходить обследование. И даже если врач говорит о возможном инфицировании плода, не стоит паниковать раньше времени. Своевременная диагностика и современная медицина в большинстве случаев оказывают положительное влияние как на здоровье будущей мамы, так и на здоровье новорождённого. И даже при внутриутробных инфекциях рождаются абсолютно здоровые малыши.
Симптомы
Для всех ВУИ есть ряд общих симптомов. Схожесть симптомов связана с несколькими моментами: особенности возбудителей — чаще внутриклеточные инфекции, организм не может самостоятельно элиминировать инфекции — как следствие персистирующее течение. Кроме того у новорождённых возрастная слабость иммунитета, из-за чего инфекции принимают медленное течение. В результате действия инфекции на плод возникает комплекс воздействий таких как гипертермия, патологическое действие микроорганизмов и их токсинов вследствие чего происходит нарушение процесса плацентации и нарушения обменных процессов[6]. [7]
- Проявления инфекции определяется сроком инфицирования плода в первые 2 недели после зачатия — бластопатия, чаще заканчивается спонтанным абортом на очень раннем сроке
- со 2 по 10 неделю беременности — истинные пороки развития вследствие поражений на клеточном уровне.
- с 10 по 28 неделю беременности — ранние фетопатии. Плод на внедрение инфекции может ответить генерализованной воспалительной реакцией (ярко выражены 1-я и 3-я фаза воспаления, альтерация и пролиферация и фиброз, а 2-я фаза — экссудация не выражена) вследствие чего у ребёнка формируются множественные пороки развития, например фиброэластоз.
- с 28 по 40 неделю беременности — поздние фетопатии. Плод уже может ответить полноценной воспалительной реакцией, чаще всего вовлекается несколько органов
- инфицирование во время родов — воспаление чаще одного органа — пневмония, гепатит.
Общие признаки[6]:
- задержка внутриутробного развития
- гепатоспленомегалия
- малые аномалии развития (стигмы дисэмбриогенеза) ранняя или прологнированная или интенсивная желтуха
- сыпи различного характера
- синдром дыхательных расстройств
- сердечно-сосудистая недостаточность
- тяжёлые неврологические нарушения
- лихорадочные состояния в первые сутки жизни
Краснуха
Вирус краснухи представляет, пожалуй, наибольшую опасность для эмбриона и плода с точки зрения возникновения аномалий развития и существенного повреждения плода. Риск заражения краснухой беременной отмечается при отсутствии в крови матери антител к вирусу краснухи. Если заболевание краснухой происходит в первые 2 месяца беременности, то вероятность инфицирования эмбриона достигает 80%, а возникновение аномалий развития возможно с вероятностью 25%. Заражение эмбриона вирусом краснухи может привести к его гибели или приводит к формированию врожденных пороков сердца, глухоты, катаракты, микроофтальмии, хориоретинита и микроцефалии. Инфицирование плода в более поздние сроки может сопровождаться появлением у новорожденного типичных кожных высыпаний, которые исчезают через некоторое время.
Принимая во внимание высокий риск возникновения аномалий развития при заболевании в первые 2-3 месяца беременности, ее необходимо прерывать. Ребенок, который родился у женщины, перенесшей во время беременности краснуху, сам является носителем вируса, и поэтому необходима его изоляция. В случае контакта беременной с больным краснухой, если она не болела ею ранее, необходима вакцинация, но не ранее 8-10 недели беременности, так как с этой целью используют живую ослабленную вакцину, и возможно негативное влияние на эмбрион.
Диагностика
Диагностика ВУИ включает два обязательных компонента: 1) уточнение характера (этиологии) инфекции и 2) доказательство внутриутробного генеза заболевания. Диагностика ВУИ крайне затруднительна. Данные анамнеза и особенности течения беременности могут позволить лишь предположить возможность внутриутробного инфицирования. Точная диагностика предполагает исследование 1) матери, 2) последа и 3) плода (новорождённого, ребёнка). Исследование последа (плаценты, оболочек и пуповины) должно быть качественным, что предполагает изучение не менее 2-х кусочков пуповины, 2-х роликов оболочек (скрученных от места разрыва до места прикрепления к плаценте) и 10 кусочков плаценты. Необходимо проведение бактериологического и иммуногистохимического (ИГХ) исследований плаценты и оболочек. Внедрение ИГХ исследований в практику патологоанатома является совершенно необходимым. Только так можно преодолеть существующую гипердиагностику хламидиоза, микоплазмоза, токсоплазмоза, «дээнковой» и других инфекций. Метод иммунофлюоресценции при исследовании последа даёт большое количество ложноположительных результатов. Методы лабораторной диагностики ВУИ можно разделить на прямые и непрямые.
К прямым относят:
- микроскопия
- культуральный метод, репликация вируса на тканях
- Выявление антигенов РИФ, ИФА и ИГЦХ.
- ПЦР[8]
Непрямые методы диагностики — это серологические исследованя методом иммуноферментного анализа (ИФА) качественный и количественный анализ IgM, IgG, IgA. У новорождённого исследуют кровь. Наличие IgG может говорить о трансплацентарном заносе антител материнских, поэтому кровь новорождённого исследуют повторно через 3-4 недели. диагностически значимым является увеличение титра IgG в 4 рза и более[9]. Обнаружение в крови новорождённого IgM говорит о наличии активной инфекции у ребёнка. Из дополнительных исследований — в общем анализе крови можно обнаружить лейкоцитоз со сдвигом влево, лейкоцитоз с нейтропенией, токсическую зернистость нейтрофилов, анемию. Кроме того, детям с подозрением на ВУИ необходимо провести УЗИ брюшной полости для выявления гепатоспленомегалии, нейросонографию[10][11].
Леченье — свет, а нелеченье — тьма. Заболевания, грозящие внутриутробным инфицированием плода
Миллиарды самых разных бактерий, кокков, грибков и прочих представителей микромира, считающихся относительно безобидными, обитают в кишечнике, бронхолегочной, мочеполовой и других системах человека. Тысячи других микробов (в том числе и тех, которые считаются возбудителями инфекционных болезней) едва ли не ежедневно вторгаются в человеческий организм извне. Иммунная система взрослого человека жестко контролирует деятельность и первых, и вторых – с более или менее безвредными микробами она поддерживает «вооруженное перемирие», ну а болезнетворным дает немедленный и жестокий бой – на войне как на войне. В общем, здоровый человек обычно не задумывается над тем, как именно складываются отношения его организма с микробами. Если, конечно, этот здоровый человек – не женщина, ожидающая ребенка.
Именно во время беременности проблема даже совершенно бессимптомного инфицирования женского организма микробами приобретает особое значение. Не говоря уже об инфекционных заболеваниях, перенесенных женщиной на разных сроках беременности. Ситуация действительно непроста — с одной стороны, внутриутробное инфициро- вание плода (вполне реальное, если женщина является носителем патогенных микробов) и вправду может привести к неблагополучному исходу беременности. С другой стороны, риск такого исхода далеко не всегда так велик, как это склонны представлять себе многие будущие мамы после лаконичного разговора с врачом в женской консультации. Так что же делать женщине, планирующей беременность, и женщине, уже ожидающей ребенка, в случае если анализы оказались «плохими»? Давайте попробуем разобраться с этой проблемой вместе.
В норме плод практически стерилен – иммунная система матери и плацента с оболочками более или менее надежно предохраняют его от преждевременной встречи с микробами. Когда эти барьеры оказываются несостоятельными, наступает собственно внутриутробное (врожденное) инфицирование. Этим термином обозначают заражение какими-либо микроорганизмами плода, находящегося в матке или продвигающегося по родовым путям, – в последнем случае плацента и плодные оболочки, разумеется, уже не защищают ребенка от инфицирования. Передача инфекции плоду может осуществляться двумя основными путями – гематогенным и восходящим. При гематогенном инфицировании возбудитель заносится материнской кровью в плаценту, а оттуда через пуповину попадает в организм плода. При восходящем же инфицировании возбудитель поднимается из половых путей матери в полость матки, инфицирует плодные оболочки, затем размножается в околоплодных водах и с ними проникает в желудочно-кишечный тракт или дыхательные пути плода. Возможно и прямое контактное заражение.
Последствия для плода зависят от многих условий – срока беременности, например. Равно как и от состояния материнского иммунитета, призванного противостоять микробной экспансии. Ну и от свойств самих микробов, конечно же.
Массивное инфицирование зародыша на ранних сроках (с 5-6-го дня до 12-й недели) зачастую приводит к его внутриутробной гибели и последующему самопроизвольному выкидышу. Это происходит из-за вызванных микробами тяжелых пороков развития плода или грубой недостаточности работы так называемых провизорных органов – хориона (наружной зародышевой оболочки), плаценты и др. Причем в данном случае вид микроорганизма особой роли не играет (за редким исключением).
При более легком инфицировании на таких ранних сроках некоторые микробы могут вызывать совместимые с жизнью пороки развития органов и тканей плода, после рождения слабо поддающиеся лечению. Еще раз подчеркнем – в данном случае речь может идти лишь о некоторых микробах. Таких, как вирус краснухи, в частности. Будущим мамам следует знать: для подавляющего большинства микробов способность вызывать уродства у плода в случаях легкого инфицирования научно доказанным фактом не является. И потому любые разговоры о «высоком» риске возникновения уродств у плода здесь совершенно неоправданны.
Инфицирование любыми микробами, произошедшее на более поздних сроках (во втором и третьем триместрах), как правило, уже не бывает причиной грубых пороков развития у плода, поскольку его органы и системы в основном сформированы. Но инфекционный процесс может вызвать микробное поражение органов и тканей малыша, а также воспаление плаценты (плацентит) и оболочек плаценты (хориоамнионит). В таких случаях вероятны преждевременные роды, а также рождение больных и ослабленных детей. Характер проблем, выявляемых у внутриутробно инфицированных малышей, весьма сильно зависит от свойств микробов, проникших в организм плода.
Ниже мы рассмотрим возбудителей некоторых наиболее распространенных инфекционных заболеваний человека, вызывающих внутриутробные инфекции. Предупреждаем заранее: мы собираемся «познакомить» вас лишь с весьма небольшой частью огромного мира микроорганизмов. В частности, вне поля зрения этой статьи вполне сознательно оставлены уже упоминавшийся вирус краснухи, токсоплазма, цитомегаловирус и вирус простого герпеса – эти возбудители уже были подробно описаны в статье о TORCH-инфекциях, ранее опубликованной в журнале (№4 за 2001 г.). Не будут упомянуты и возбудитель сифилиса и гонококк – эти инфекции заслуживают отдельного рассказа. Еще одному из «исключенных» микробов – вирусу гриппа – также будет отведено «почетное» место в одном из ближайших номеров журнала.
Хотелось бы напомнить: все лекарственные препараты и лечебные процедуры назначает лечащий врач. Самолечение, как известно, – зло. Самолечение во время беременности – двойное зло. Оно может повлечь очень тяжелые последствия как для ребенка, так и для матери!
Микоплазмы
Микоплазмы – это самые мелкие из существующих в природе организмов, способных самостоятельно жить и размножаться. В группу микоплазм входят два рода микроорганизмов – собственно микоплазма и уреаплазма.
Собственно микоплазма. Два из трех видов патогенных (болезнетворных) микоплазм передаются при сексуальном контакте (урогенитальный микоплазмоз), один – воздушно-капельным путем (респираторный микоплазмоз). Микоплазмы «в союзе» с другими микроорганизмами могут вызывать у взрослых самые разнообразные заболевания – они паразитируют в мочеполовых органах и в органах дыхания, вызывая вагиниты, сальпингиты, пиелонефрит, мужское бесплодие, пневмонию, ОРЗ. Заболевания, вызываемые микоплазмами «в чистом виде», протекают, как правило, малосимптомно или даже бессимптомно – некоторые ученые даже сомневаются в способности этих микробов вообще вызывать болезни. Методы диагностики микоплазменных инфекций – посев на питательные среды, иммуноферментный анализ (ИФА), ДНК-диагностика.
Во время беременности латентная (бессимптомная) микоплазменная инфекция иногда активизируется. Внешне это может проявиться симптомами воспаления мочеполовой системы – усилением выделений из влагалища, резями и жжением при мочеиспускании, тянущими болями внизу живота и т.д. В содружестве с другими микробами «разгулявшиеся» микоплазмы вполне способны вызывать воспаление плодных оболочек, что в конечном итоге может привести к преждевременным родам. При обследовании новорожденного могут быть обнаружены признаки микоплазменной инфекции – иногда весьма тяжелой (вплоть до воспаления мозговых оболочек и общего заражения крови). Но это бывает весьма редко, причем обычно поражение органов и систем ребенка обусловлено не только микоплазмой, но и микробами, активизировавшимися одновременно с ней.
Некоторое время назад отечественными учеными предполагалась связь между микоплазменной инфекцией во время беременности и развитием у плода врожденных уродств. Однако убедительных доказательств справедливости этой гипотезы у мировой науки нет и по сей день.
Микоплазменные инфекции лечатся антибиотиками. Врач назначает лечение индивидуально – у беременной женщины оно зависит от срока и особенностей протекания беременности. В частности, антибиотикотерапию назначают лишь после 12 недели беременности, при этом предпочтение отдается препаратам, наименее токсичным для плода, например «Зитромаксу» или эритромицину.
Уреаплазма. Уреаплазмоз обычно протекает как хроническая инфекция мочеполовых путей. Женщины чаще всего бывают бессимптомными носителями уреаплазмы. Для диагностики уреаплазмоза используют практически те же лабораторные методы, что и для обнаружения микоплазм.
Внутриутробно плод инфицируется уреаплазмой в редчайших случаях, поскольку, как правило, этот микроб через плаценту не проникает. А вот во время родов, проходя по родовым путям инфицированной матери, ребенок заражается в 50% случаев. Чтобы свести риск к минимуму, уреаплазмоз лечат во время беременности – обычно после 12-й недели. Антибактериальные препараты (чаще всего – все те же «Зитромакс» и эритромицин) назначает лечащий акушер-гинеколог.
Хламидии
По своим свойствам хламидии занимают промежуточное положение между вирусами и бактериями. Механизм передачи хламидиоза – половой, восприимчивость людей к этой инфекции довольно высока. Иммунитет к хламидиозу не вырабатывается, поэтому возможно повторное инфицирование. Инкубационный период составляет приблизительно 1-3 недели. При заболевании могут наблюдаться характерные стекловидные выделения из мочеиспускательного канала – чаще по утрам. Иногда возникает зуд или неприятные ощущения при мочеиспускании, общая слабость, незначительное повышение температуры. Однако следует отметить, что в большинстве случаев болезнь протекает в бессимптомной или слабовыраженной форме.
Хламидиоз достаточно часто осложняется вялотекущими воспалительными заболеваниями мочеполовой сферы. У женщин это эндометриты, сальпингиты, цервициты, непроходимость фаллопиевых труб (и как следствие – внематочная беременность или бесплодие). Помимо мочеполовой системы, хламидиоз может поражать и другие органы – при переносе возбудителя (например, грязными руками) с отделяемым из мочеполовых органов на слизистую оболочку глаз, носоглотки.
Во время беременности хламидии могут вызывать проблемы, весьма схожие с последствиями микоплазменной инфекции, но в чуть более мягкой форме. Это обусловлено тем, что хламидии реже кооперируются с другими микробами – они вполне способны вызвать заболевание и «в одиночку». Самым частым проявлением врожденной хламидийной инфекции у малышей являются конъюнктивиты (воспаление слизистой глаз). Возможны и более тяжелые поражения – но, к счастью, они очень редки.
Диагностика хламидиоза во время беременности может проводиться разными методами – при помощи иммуноферментного анализа и прямой иммунофлюоресценции, полимеразной цепной реакции, посевов на специальные питательные среды и т.д.
Лечение хламидиоза достаточно сложно и трудоемко. Помимо антибактериальной терапии (эритромицин, амоксициллин – но не фторхинолоновые препараты, обычно используемые при лечении взрослых!), оно обычно включает в себя другие медикаментозные методы, а также диету и отказ от половой жизни на время лечения. Лечить непременно нужно обоих половых партнеров. По окончании курса проводятся повторные анализы. Если хламидии не обнаружены, анализы повторяют еще два раза с интервалом в месяц.
Бактерии
Из этой очень большой группы микроорганизмов коротко остановимся только на возбудителе листериоза. Это инфекционное заболевание вызывается бациллой с названием листерия. Природным «резервуаром» инфекции служат грызуны, а также некоторые домашние животные. Основных путей заражения два – «алиментарный» (т.е. микробы попадают в организм человека с пищей, ими же загрязненной) и внутриутробный (врожденный листериоз). В развитии инфекции большую роль играет состояние иммунной системы человека. Различают множество форм листериоза, поэтому говорить о его симптоматике в научно-популярной статье, пожалуй, не имеет смысла – это скорее тема отдельной монографии.
Важно отметить, однако, что среди различных форм листериоза специально выделяют «листериоз беременных». Обследование большого числа женщин – матерей детей с врожденным листериозом показало, во-первых, что у большинства из них во время беременности не было типичных проявлений листериозной инфекции, а во-вторых, что далеко не всякое бактерионосительство приводит к внутриутробному инфицированию плода. При заражении плода во время беременности, как правило, развивается острый хориоамнионит, приводящий к мертворождению или преждевременным родам, инфекционному поражению многих органов и систем плода. При заражении новорожденного во время родов признаки врожденного листериоза проявляются через 1-2 недели после родов. Болезнь нередко протекает весьма тяжело, листерии могут обусловить бронхо-пневмонию, увеличение печени, желтуху и другие серьезные заболевания и симптомы.
Думаю, прочитавших эти строки не нужно убеждать в том, что листериоз беременных очень опасен для плода. Поэтому исключительно важна ранняя диагностика этого достаточно коварного заболевания. В каких же случаях будущей матери стоит насторожиться? При часто повторяющихся ангинах, воспалении яичников, шейки матки, при наличии в прошлом нескольких выкидышей или мертворождений. Если женщина беременна, к перечисленным показаниям можно добавить и патологическое течение беременности. Для диагностики листериоза на исследование обычно берут образец крови, а также слизи из носоглотки и зева (при симптомах ангины). Беременным женщинам чаще всего назначают антибактериальное лечение пенициллином и другими представителями этого относительно безопасного для здоровья плода семейства антибиотиков.
Простейшие
Наиболее значимые представители этой группы – токсоплазмы и трихомонады. О токсоплазмах было подробно рассказано в предыдущем номере журнала.
Трихомонады способны вызывать целый комплекс воспалительных заболеваний мочеполовой сферы, называемый единым термином трихомоноз. У женщин это могут быть вульвиты, кольпиты, цервициты, бартолиниты и т.д. Заражение обычно происходит при половом контакте. Между «роковым» половым актом и появлением первых признаков заболевания может пройти от 4 дней до 4 недель (чаще всего – около недели). Женщины нередко ощущают тяжесть в нижней части живота, зуд и жжение во влагалище. Нередко из влагалища выделяется белесая жидкость с неприятным запахом – бели. Впрочем, зачастую заболевание протекает малосимптомно (наблюдаются только бели) или вообще бессимптомно. Диагноз устанавливается на основании анализа выделений из половых органов. Как правило, здоровый организм избавляется от трихомонад собственными силами, поэтому болеют в основном люди, по тем или иным причинам ослабленные, либо ведущие уж очень беспорядочный образ жизни. Однако не стоит относиться к трихомонадам чересчур благостно: внутри этих простейших нередко «прячутся» другие – зачастую куда более грозные – «злодеи». Например, возбудители сифилиса и гонореи.
Во время беременности активно размножающиеся в организме женщины трихомонады могут представлять серьезную опасность для плода. Распространяясь восходящим путем до уровня матки, этот микроб способен вызывать выраженное воспаление оболочек плода (хориоамнионит), подчас приводящее к тяжелым последствиям – вплоть до выкидыша и мертворождения. К счастью, такой исход является редкостью, его вероятность относительно высока только в случаях запущенного, неадекватно леченного трихомоноза.
Для лечения трихомоноза во время беременности обычно используют метронидазол (трихопол). Хотя этот препарат и не относится к совершенно безобидным для плода (особенно в первом триместре беременности), назначение его при данной инфекции вполне оправдано. Однако, конечно же, не в плане самолечения! Любые медикаменты во время беременности должны назначаться врачом – после тщательного анализа всех показаний и противопоказаний к их употреблению.
Грибы
Самый частый «виновник» инфекционных проблем во время беременности (из этой группы микробов) – дрожжевой грибок с весьма поэтическим названием «белая кандида».
Этот гриб вызывает инфекционную болезнь, называемую кандидамикоз (или кандидоз), в народе более известную как «молочница». Кандидамикоз – достаточно распространенное среди женщин (в том числе и беременных) заболевание. Вообще-то этот грибок – частый спутник человека. Даже у совершенно здоровых людей какое-то количество кандиды паразитирует на слизистых оболочках некоторых органов. Но если иммунная система работает в полную силу, защитные механизмы не позволяют грибку оказывать вредное действие. В случаях, когда организм человека ослаблен, зловредный грибок может безнаказанно вести «подрывную деятельность». В половые пути женщины кандида заносится грязными руками, инфицированными предметами, иногда – половым путем. Там она начинает активно делиться, вызывая воспаление влагалища, шейки матки, мочеиспускательного канала. Один из самых распространенных симптомов кандидамикоза – зуд и обильные выделения из влагалища.
У беременных женщин кандидамикоз встречается в 2-3 раза чаще, чем у небеременных. Дело в том, что во время беременности химическая среда во влагалище становится более кислой – и это очень «нравится» кандиде. В то же время гормональные изменения в организме ведут к снижению клеточного иммунитета и активности лейкоцитов, что также способствует усиленному размножению грибка в половых путях будущей матери. Заражение плода обычно происходит восходящим путем. Возбудитель может поражать многие органы и системы плода, но чаще ограничивается пуповиной, кожными покровами, слизистой рта и бронхолегочной системой. При значительном распространении микроба последствия для плода могут быть тяжелыми (вплоть до гибели).
Диагноз «кандидамикоз» подтверждается или исключается микроскопическим исследованием мазка, взятого из половых путей женщины.
Во время беременности кандидамикоз, в принципе, лечится так же, как и при ее отсутствии. Однако важно знать, что ряд препаратов, успешно применяемых в прочих случаях, беременным противопоказан: это касается подавляющего большинства противогрибковых средств, выпускаемых в виде пероральных таблеток и растворов для инъекций. Вместо таковых обычно используются препараты для местного применения – мази, кремы и другие «наружные» лекарственные формы, содержащие клотримазол, миконазол или натамицин.
Конечно, в рамках одной статьи невозможно сколько-нибудь полно осветить такую серьезную проблему, как внутриутробное инфицирование. Но, думается, кое-какую пользу вышеприведенная информация будущим мамам все же принесет – по крайней мере, общепринятые в мировой медицине рекомендации по борьбе с внутриутробной инфекцией многим из них станут понятнее, чем раньше.
Смысл же этих рекомендаций несложен: профилактика и еще раз профилактика.
Во время подготовки к беременности и ее вынашивания будущим родителям следует предпринять максимум мер по предупреждению развития инфекции в организме женщины. В идеальном варианте каждой супружеской паре, еще только планирующей деторождение, не мешало бы обследоваться на предмет носительства потенциально вредных для плода микробов – благо, современные диагностические методы позволяют быстро и точно определить факт инфицированности супругов и назначить адекватное лечение. Прицельно подобранные антибиотики, вакцины, иммуноглобулины, препараты интерферона и его индукторы, противовирусные, антипротозойные и другие средства помогут изгнать инфекцию из организма еще до зачатия. Для этого необходимо и достаточно лишь своевременно обратиться к соответствующему специалисту. Следует также помнить, что упорядоченная половая жизнь и техника безопасного секса существенно уменьшает вероятность заражения болезнями, передаваемыми половым путем, – и во время беременности этот факт даже более актуален, чем вне таковой.
Не следует пренебрегать регулярным медицинским обследованием и во время беременности – назначаемые врачом акушером-гинекологом анализы позволят своевременно обнаружить присутствие в организме женщины микробов, потенциально опасных для плода. И если это случилось, ни в коем случае не следует поддаваться панике. Во-первых, потому что риск тяжелых последствий для плода чаще всего невысок. А во-вторых, потому что в арсенале современной медицины вполне достаточно лекарственных средств и лечебных методик для того, чтобы сделать этот риск еще более низким. Об опасности внутриутробного инфицирования непременно следует помнить. Но не следует перед этой опасностью пасовать. И тогда все будет хорошо.
Клинические формы
Неонатальный герпес
| ВУИ: неонатальный герпес | |
| МКБ-10 | 35.235.2 |
| МКБ-9 | 771.2771.2, 054.xx054.xx |
| MeSH | D018445 |
Из вирусов семейства герпеса все основные типы могут вызывать герпетическую инфекцию у новорождённого: вирус простого герпеса 1 и 2 типа, вирус простого герпеса 3 типа (varicella zoster), 4 тип — Вирус Эпштейна — Барр, волосистая лейкоплакия языка, синдром иммунной депрессии, 5-й тип — цитомегаловирусная инфекция, 6-й тип — розеола, 7-й тип — синдром хронической усталости, 8-й тип — саркома Капоши. Однако термин «неонатальный герпес» употребляется только применительно к заболеваниям, вызванным вирусом простого герпеса 1 и 2 типа. Самым опасным для ребёнка является ВПГ-2.
Вероятность инфицирования ребёнка зависит от того, насколько давно инфицирована мать. Чем «свежее» инфекция — тем больше шансов заразиться у ребёнка. Если к моменту родов у матери есть высыпания — это показание для кесаревого сечения[12].
Клинические проявления
- 1. Локальная форма (кожно-слизистая) — поражение кожи, слизистых, реже энцефалит.
- 2. Церебральная форма — клиническая картина соответствует общим признакам ВУИ, но есть и специфические признаки: поражение глаз и слизистых; герпетический энцефалит, который носит некротический характер, в результате чего разрушение мозга может быть вплоть до полушарий; выраженная тромбоцитопения с геморраческим синдромом.
- 3. Диссеминированный неонатальный герпес
Диагностика
В диагностике неонатального герпеса имеет значение оценка специфического анамнеза матери. При клиническом осмотре детей, родившихся от матерей с острым или рецидивирующим генитальным герпесом, осмотр кожи и слизистых необходимо производить с особой тщательностью. При возникновении у новорождённого судорог неясной этиологии показано проведение люмбальной пункции (при герпетическом энцефалите отмечается лимфоцитоз, моноцитоз и высокая концентрация белка). При возникновении у новорождённого клиники сепсиса, при котором нет эффекта от антибиотиков — необходимо обследование на герпес. Среди лабораторных методов диагностики золотым стандартом является выделение вируса из крови, ликвора, везикул культуральным методом. При кожной форме можно исследовать содержимое везикул или соскоб с кожи иммунофлуоресцентным методом с целью обнаружения антигена вируса. А при генерализованной инфекции и менингоэнцефалите исследуют кровь и ликвор методом ПЦР. Уровень антител IgG не информативен, так как это антитела матери. Уровни IgM говорят об острой инфекции у новорождённого.
Лечение
При всех формах неонатального герпеса показана системная противовирусная терапия, так как локализованная форма может предшествовать генерализованной. При раннем назначении противовирусных препаратов исход благоприятный. Независимо от формы инфекции применяют ацикловир. Ацикловир (Зовиракс, Виролекс) в\в 2-3 недели плюс противогерпетический иммуноглобулин 2 — недели[12]. Прекращать грудное вскармливание не имеет смысла, так как проникновение ВПГ в молоко матери маловероятно, за исключением высыпаний на груди у матери. Из местных средств при офтальмогерпесе применяется видарабин, флореналь, бонафтоновая мазь.
Врождённая цитомегаловирусная инфекция
Частота встречаемости 0,2-2,5 %. Вирус передается всеми секретами (слюна, моча, кровь, слезы). Клинические проявления при первичном инфицировании у беременных неспецифичны, могут напоминать клинику ОРВИ. Есть ряд факторов, способствующих высокой частоте внутриутробного инфицирования вирусом цитомегалии. К ним относятся эпидемиологические особенности, такие как значительная генетическая вариабельность штаммов ЦМВ, широкое распространение ЦМВ-инфекции в человеческой популяции (в подавляющем большинстве — в виде латентно-персистирующего течения), преобладание субклинических форм, как при первичной, так и при вторичной инфекции, разнообразие механизмов и путей передачи инфекции. Следующим фактором является незрелость иммунитета плода и новорождённого. И наконец, адаптационные иммунные изменения в организме женщины во время беременности (снижение функциональной активности клеточных механизмов иммунитета), при которых возможна реактивация латентно-персистирующей ЦМВ-инфекции.
Заражение чаще всего происходит в родах, или с молоком матери. Во время беременности заражение происходит только в том случае, если мать впервые инфицируется во время беременности.
Клинические проявления
Врождённый гепатит с выраженной желтухой, тяжёлая тромбоцитопения с геморрагическим синдромом, менингоэнцефалит. Специфические признаки — кальцификаты в субэпендимальных отделах мозга и хориоретинит. Отдаленный прогноз определяется степенью поражения головного мозга. Если рано перенесённый менингоэнцефалит — дети как правило инвалиды, если гепатит — рано развивается цирроз, если кардит — хроническая сердечная недостаточность.
Диагностика
Обследованию на ЦМВ-инфекцию подлежат дети, имеющие симптоматику врождённой инфекции, а также без клинических проявлений TORCH-синдрома, если они рождены женщинами из группы риска. У новорождённых детей в раннем неонатальном периоде при подозрении на ЦМВ прежде всего проводят идентификацию возбудителя любым доступным способом. Чаще всего используется ПЦР или выявление антигенов вируса, реже используется вирусологический метод. Материалом для ПЦР может служить любая биологическая жидкость (моча, слюна, кровь, слезы), однако об активной ЦМВ-инфекции говорят только при обнаружении методом ПЦР генома ЦМВ в крови и ликворе. При нахождении ДНК вируса в других средах однозначную оценку периоду заболевания дать нельзя. Для уточнения остроты процесса используют серологические методы — определяют анти-цитомегаловирусные антитела классов М и G. Причём обязательно исследование «парных сывороток», то есть контроль исследования титров антител через 3-4 недели. Выявление антител класса IgM в пуповинной крови и в крови ребёнка в первые недели жизни является важным диагностическим признаком. А выявление IgG в крови ребёнка без сопоставления с материнскими титрами не является диагностически значимым, так как возможен трансплацнтарный перенос антител из организма матери.
Лечение
Терапия врождённой ЦМВ-инфекции складывается из этиотропной и синдромальной терапии. Показанием к проведению этиотропной терапии является активный период врождённой ЦМВ-инфекции. Препаратом для выбора этиотропного лечения является цитотект. Детям вводят антицитомегаловирусный иммуноглобулин (цитотект) внутривенно 2 мл/кг 2 раза в день каждые 2 дня в течение 3 недель[13].
Если есть опасность для жизни, то добавляют ганцикловир в/в на 14-21 день, хотя виростатики (противовирусные препараты) типа ганцикловира, фоскарнета применяются крайне редко из-за их высокой токсичности.
Врождённый токсоплазмоз
Частота 1:1000 новорождённых Ооцисты токсоплазм обычно находятся в фекалиях кошек и коз, откуда попадают во внешнюю среду. У беременных клиника заболевания протекает по типу мононуклеоза или гриппа, с высокой температурой или очень длительным субфебрилитетом, увеличены лимфоузлы. Часто присоединяется артралгия или артрит.
Вероятность инфицирования плода: заражение обычно происходит если инфекция свежая и зависит от срока инфицирования. Если 1 триместр — вероятность 15 %, во второй 30 %, в третий — 60 %.
Клинические проявления
У плода и новорождённого инфекция может быть в двух формах: поражение глаз и головного мозга или генерализованный токсоплазмоз. Помимо общих признаков инфекционного токсикоза присоединяется гепатит, менингоэнцефалит, поражение глаз (врождённая катаракта, может быть глаукома, атрофия зрительного нерва).
Диагностика
Схема обследования на токсоплазмоз новорождённых детей: при наличии клинических признаков токсоплазмоза исследуют антитела. Если антитела не обнаружены — исследование повторяют через 2 недели, если при повторном исследовании антител нет — то дальнейший контроль не нужен. При обнаружении показана специфическая терапия. Если при первичном исследовании обнаружены антитела класса IgM, то сразу показана этиотропная терапия. Если обнаружены только IgG, то исследование повторяют через 4 недели. Терапия показана при нарастании титра антител. При падении титра ребёнок в лечении не нуждается, но дальнейший контроль необходим.
Лечение
Лечение токсоплазмоза может проводиться антенатально — то есть лечение беременной женщины. Если инфицирование в 1-й половине беременности — применяют спирамицин, клафоран, ровамицин. Если во 2-ю половину беременности — хлоридин + сульфасалазин + фолиевая кислота. Лечение детей эффективно в периоды циркуляции в крови внецистных форм паразита, на цистные формы препараты не действуют. В полной санации нет необходимости, так как цистные формы (носительство) обеспечивает нормальный нестерильный иммунитет. Наиболее эффективны препараты пириметамина в комбинации с сульфаниламидами. Имеются комбинированные препараты: фансидар, метакельфин. Также применяют ко-тримоксазол в возрастной дозировке[14]. Лечение новорождённых предполагает следующую схему: хлоридин + сульфадимезин + фолиевая кислота. Курс 4-6 недель. В течение первого года 4 курса с перерывом 1,5 месяца, а в перерыве спирамицин в течение 1,5 месяцев[12][15][16].
Хламидиоз
Данные ВОЗ свидетельствуют о том, что у 35-50 % новорождённых, матери которых инфицированы C. trachomatis
, развивается хламидийная офтальмия (в 5 раз чаще гонококковой), у 11-20 % — пневмония[17]. Инфицирование как правило происходит в родах, вероятность передачи 40-70 %. Заболевание проявляется не сразу, а спустя 7-14 суток.
Клинические проявления
Существуют три формы инфекции у новорождённых:
- персистирующая
- латентная
- острая (генерализованная инфекция — менингоэнцефалит, внутриутробная пневмония, гастроэнтерит)[17][18].
Основными проявлениями заболевания у новорождённого являются:
- назофарингит 25 %
- конъюнктивит устойчивый к применению обычных средств, отвечает только на терпию тетрациклиновой мазью,
- пневмонии 10-15 %- нерезковыраженный токсикоз, но резко выраженный обструктивный синдром, приступообразный мучительный кашель.
- высокая эозинофилия
- проктиты, гастроэнтериты — 5 %
- вульвиты, уретриты 15 %
Лечение
Необходимо кроме ребёнка лечить и папу и маму. Новорождённому ребёнку назначают эритромицин в свечах на 24 дня или эригран внутрь. Также можно использовать Азитромицин[12][19].
Микоплазмоз
Инфицирование микоплазмой как правило происходит в родах. Частота выявления возбудителя у беременных — 20—50 %, риск инфицирования плода не известен. Проводят терапию беременных с серопозитивным микоплазмозом после 16-й недели беременности, что снижает частоту заболеваемости новорождённых.
Клинические проявления
У новорождённых проявляется в виде пневмонии, которая начинается незаметно с токсикоза, появляется бледность, нарастает одышка, а только потом появляются физикальные данные. На рентгенограмме специфичным признаком являетс «симптом снежной бури» — двухсторонняя мелкоочаговая, местами сливная пневмония. Летальность составляет 15 %.
Лечение
Новорождённым назначают эритромицин или азитромицин, а при тяжёлых формах левомицетин[20][12].
Синдром врождённой краснухи
| Внутриутробные инфекции | |
| Катаракта при синдроме врождённой краснухи | |
| МКБ-10 | 35.035.0 |
| МКБ-9 | 771.0771.0 |
| DiseasesDB | 11729 |
| MedlinePlus | 001658 |
| eMedicine | emerg/388 |
| MeSH | D012410 |
Если мать инфицируется в первые 12 недель то беременность лучше прервать. До беременности необходимо обследоваться, и если мать серонегаттивна — то вакцинироваться[12]. Если мать заражается краснухой в 1 триместре — вероятность у ребёнка 25 %, после 5-го месяца — 1-2 %.
Клинические проявления
Характерным клиническим проявлением является триада Грега
:
- врождённый порок сердца по типу открытого артериального протока, дефекта межжелудочковой перегородки, дефекта межпредсердной перегородки, стеноза легочной артерии, некроза миокарда
- пороки глаз (катаракта, микрофтальмия, глаукома)
- глухота.
У 2\3 детей врождённая краснуха проявляется по окончании перинатального периода.
Лечение
Специфической терапии не существует, лечение симптоматическое.
Кандидоз новорождённых
Частота кандидоза в структуре инфекционно-воспалительных болезней новорождённых около 15—30 % случаев, причём в половине из них он остаётся нераспознанным или поздно диагностируемым[21]. Кандидоз может быть вызван любым из видов, но чаще всего Candida albicans. К факторам риска развития кандидоза у новорождённых относятся: недоношенность, сахарный диабет у матери во время беременности, урогенитальный кандидоз матери во время беременности, повторные курсы антибиотиков, особенно в сочетании с иммуносупрессивной терапией, нарушения иммунитета, особенно нейтропения, наличие в раннем неонатальном периоде ИВЛ, реанимационных мероприятий, полостных операций.
Клинические проявления
По времени инфицирования выделяют врождённый
кандидоз, который развился при антенатальном или интранатальном инфицировании и
постнатальный
кандидоз. В зависимости от локализации процесса кандидоз делят на:
- кандидоз кожи — поражение кожи и её придатков. Может быть локализованное или распространённое поражение.
- кандидоз слизистых оболочек полости рта, конъюнктивы, наружных половых органов
- генерализованный кандидоз — поражение внутренних органов, не сообщающихся с внешней средой с присоединением кандидемии.
- висцеральный кандидоз — поражение внутренних органов и других систем, не сообщающихся с внешней средой, например кардит, гепатит, нефрит.
- системный кандидоз — поражаются один или несколько органов, сообщающихся с внешней средой — например, кандидоз желудочно-кишечного тракта.
- кандидозоносительство — присутствие Candida в естественных местах обитания в большей, чем предусмотрено концентрации.
Также кандидоз классифицируют по тяжести процесса на лёгкую
и
тяжёлую
формы в зависимости от локализации и объёма поражения, наличия инфекционного токсикоза. А кроме этого выделяют
острое
(7—14 дней) и
затяжное
(более 6 недель) течение заболевания.
Диагностика
Диагностика неонатального кандидоза базируется на клинической картине. При кожной и кожно-слизистой форме необходимости в лабораторном подтверждении нет. Лабораторная диагностика приобретает решающее значение при генерализованном, висцеральном и системном кандидозе. Лабораторными критериями могут считаться выявление грибов в активном состоянии при микроскопии субстрата, выделение антигенов и ДНК в стерильных субстратах, выделение в количествах больше допустимых при посеве субстратов, являющихся местом сапротифирования грибов.
Лечение
При локализованном кандидозе кожи применяется местная терапия противогрибковыми мазями (клотримазол, изоконазол, кетоконазол, натамицин). При затяжном течении назначают системные антимикотики — флуконазол внутрь. Суточная доза 5-8 мг\кг один раз в сутки. При кандидозе слизистых пораженные участки обрабатывают 2 % раствором соды или 0,1 % раствором гексорала. При рецидивировании применяют флуконазол. При системных кандидозах для лечения ЖКТ, дыхательной, мочеполовой системы, а также при висцеральном и генерализованном кандидозе лечение начинают с назначения флуконазола, а при неэффективности в течение 5—7 дней назначают амфотерицин В или амбизом в/в капельно[22].
Ранний врождённый сифилис
На фоне эпидемического роста заболеваемости сифилисом в России в 90-х годах резко выросла заболеваемость врождённым сифилисом: в 1997 г. общая заболеваемость сифилисом превысила уровень 1990 г. в 51 раз, врождённым сифилисом — в 47 раз. Динамика роста заболеваемости врождённым сифилисом аналогична динамике удельного веса беременных среди больных сифилисом женщин. По данным Л. И. Тихоновой (1999 г.), в 1995-97 гг. в России этот показатель постоянно рос: 4,9 %, 5,5 %, 6,5 %[23].
Врождённый сифилис можно предупредить путём выявления и лечения зараженных матерей во время беременности. Поэтому беременных трёхкратно обследуют серологически, в том числе непосредственно перед родами.
Ранний врождённый сифилис — это ВУИ, проявляющаяся у ребёнка в возрасте до 2-х лет (согласно МКБ-10). Ранний врождённый сифилис может быть манифестный
(с клиническими проявлениями) и
скрытый
.
Клинические проявления
У новорождённых детей с ранним врождённым сифилисом наблюдаются следующие симптомы: сифилитический ринит, диффузная инфильтрация Хохзингера, хориоретинит, гепатоспленомегалия, сифилитическая пузырчатка, розеолезная и пустулезная сыпь, остеохондрит, периоститы, остеопороз.
Диагностика
У новорождённых от матерей больных сифилисом при рождении берут на анализ пуповинную кровь для проведения комплекса серологических реакций. Кроме того проводят взвешивание и патоморфологическое исследование плаценты. При сифилисе плацента увеличена по массе, имеются признаки воспаления. Обязательно делают спинномозговую пункцию. В анализе ликвора присутствуют специфические изменения: лимфоцитарный цитоз выше 20 клеток в 1 мл, белок выше 1,5-1,7 г\л, положительные результаты РИФ и комплекса серологических реакций. На 7-8 сутки жизни ребёнка повторяют серологические исследования крови — реакцию микропреципитации, реакцию иммунофлуоресценции, реакцию иммобилизации бледных трепонем, иммуноферментный анализ для выявления IgM.
Лечение
Лечение проводится одним из препаратов пенициллина в течение 2-3 недель. Выбор препарата зависит от анализа ликвора. После окончания лечения ребёнка выписывают под наблюдение дерматовенеролога, а в районную поликлинику диагноз сообщается только с согласия матери. В КВД 1 раз в 3 месяца до достижения ребёнком возраста 3-х лет проводится клинико-серологический контроль[24].
Примечания
- ↑ 12В. В. Власюк
Морфологическая диагностика внутриутробных инфекций. Учебное пособие. СПб, 2010 — 47 с. ISBN — 5-00-001976-8/ - Охотникова И. М., Агейкин В. А., Лозовская Л. С. Значение внутриутробной вирусной инфекции в органной патологии детей грудного возраста // Мед. научный и учебно-методич. журнал. — 2001. — № 5. — С. 81-87.
- Врождённые пороки развития. Пренатальная диагностика и тактика / Под ред. Б. М. Петриковского, М. В. Медведева, Е. В. Юдиной. — М.: РАВУЗДПГ: Реальное время, 1999. — 325 с.
- https://spravka.komarovskiy.net/vnutriutrobnye-infekcii.html Комаровский. Внутриутробные инфекции
- https://www.ic.omskreg.ru/~medstat/BIBLIO/opport/index.htm Долгих Т. И., Носкова Ф. В. Оппортунистические инфекции у детей (вопросы диагностики, клиники и лечения). Омск: Изд-во ОГМА, 1999. — 99 с.
- ↑ 12
А. Л. Заплатников, Н. А. Коровина, М. Ю. Корнева, А. В. Чебуркин А. Л. Заплатников, Н. А. Коровина, М. Ю. Корнева, А. В. Чебуркин Лечащий врач 08-2005 https://www.lvrach.ru/doctore/2005/08/4532901/ - А. Я. Сенчук, З. М. Дубоссарская.
Перинатальные инфекции: практич. пособие. — М.: МИА, 2004. — 448 с с. - Диагностика внутриутробных инфекций у новорождённых детей методом полимеразной цепной реакции
- Внутриутробные инфекции. Симптомы. Диагностика. Профилактика. | EUROLAB | Педиатрия
- Володина Н. Н., Дегтярева Д. Н.
Диагностика и лечение внутриутробных инфекций. — М.: Метод. рек. для врачей неонатологов, 1999. - https://www.rae.ru/ru/publishing/mono07_811.html СОВРЕМЕННЫЕ ПРИНЦИПЫ ДИАГНОСТИКИ ВНУТРИУТРОБНОЙ ИНФЕКЦИИ ПЛОДА
- ↑ 123456
Перинатальные инфекции (вопросы патогенеза, морфологической диагностики и клинико-морфологических сопоставлений) Цинзерлинг В. А., Мельникова В. Ф. - Клинико-лабораторная характеристика, патоморфологические особенности, диагностика и лечение цитомегаловирусной пневмонии «Инфекционные болезни», 2004. — Т. 2, № 1. — С. 73-80. В. И. Шахгильдян, О. А. Тишкевич, О. Ю. Шипулина. https://www.hivrussia.ru/pub/2006/16.shtml
- Чебуркин А. В. Клиника и дифференциальная диагностика врождённого токсоплазмоза «Медицинская паразитология и паразитарные болезни» № 5, 1984, с. 53-57.
- О выявлении и профилактике токсоплазмоза в Москве. Методические рекомендации (№ 25). М., 2007
- Клиника, диагностика и лечение токсоплазмоза Г. Ю. Никитина, Ф. К. Дзуцева, Ю. В. Борисенко, Л. П. Иванова Лечащий врач 10-2008 https://www.lvrach.ru/doctore/2008/10/5828652/
- ↑ 12
Урогенитальный хламидиоз Chlamydial Genitourinary Infections https://www.venuro.info/venera/chlamidioz.php - Хламидиоз Усков Александр Николаевич https://queerlvov.narod.ru/hlamidioz.html
- https://www.hlamidioz.info/6.html Хламидиоз у детей
- Перинатальные инфекции: практич. пособие / под ред. А. Я. Сенчука, З. М. Дубоссарской. М.: МИА, 2005. 318 с
- Протоколы диагностики, лечения и профилактики внутриутробных инфекций у новорождённых детей, Москва, ГОУ ВУНМЦ МЗ РФ, 2001 год стр. 53
- Протоколы диагностики, лечения и профилактики внутриутробных инфекций у новорождённых детей, Москва, ГОУ ВУНМЦ МЗ РФ, 2001 год стр. 55-57
- https://www.ill.ru/news.art.shtml?c_article=142 Сифилис и беременность
- Протоколы диагностики, лечения и профилактики внутриутробных инфекций у новорождённых детей, Москва, ГОУ ВУНМЦ МЗ РФ, 2001 год стр. 59-64
Вирусный гепатит
Вирусный гепатит представляет собой тяжелое заболевание печени. В зависимости от разновидности вируса вызывающего гепатит, различают следующие их типы: гепатит А, гепатит В, гепатит С, гепатит D, гепатит Е, гепатит F и гепатит G.
Гепатит А. Заболевание вызывается РНК-содержащим вирусом. Инфекция к матери передается фекально-оральным путем. Заражение плода происходит редко. Заражение новорожденного происходит при кормлении грудью в период нахождения вируса в крови у пациентки. Инкубационный период составляет 15-45 дней. У беременной заболевание протекает обычно в легкой или в среднетяжелой форме. Отмечается тошнота, рвота, увеличение печени, желтуха, боль в правом подреберье. В связи с тем, что вирус гепатита А не проникает через плаценту, он не приводит к возникновению пороков развития у плода. Острый вирусный гепатит А излечивается после короткой вирусемической фазы, не переходит в хроническую форму и не вызывает цирроз печени. Диагностику острого гепатита А проводят путем определения специфических антител в крови, которые выявляются уже через 2 недели после инфицирования. Лечение гепатита А проводят по общетерапевтическим, симптоматическим критериям. В случае контакта беременной с больным гепатитом А с профилактической целью вводят g-глобулин.
Гепатит В в настоящее время представляет одну из важных проблем здравоохранения, что связано с увеличением частоты заболевания и с развитием неблагоприятных исходов в виде формирования хронического гепатита, цирроза печени и гепатоцеллюлярной карциномы. Возбудителем гепатита В является ДНК-содержащий вирус. Предполагается, что этот вирус является онкогенным. У беременных регистрируется 1-2 случая острого гепатита В на 1000 беременностей и 5-15 случаев хронического гепатита В. Источником инфекции являются больные с острым и хроническим гепатитом и вирусоносители. Передается вирус при переливании крови и препаратов крови, при половых контактах. Также возможно заражение при тесных бытовых контактах (использование общих зубных щеток, расчесок, носовых платков) и при использовании плохо обработанных медицинских инструментов.
В 85-95% случаев инфицирование плода происходит во время родов вследствие контакта с кровью, инфицированными выделениями родовых путей или путем заглатывания инфицированных выделений. В 2-10% случаев инфицирование происходит во время беременности путем проникновения вируса через плаценту, особенно при нарушении функции плаценты при фетоплацентарной недостаточности или при отслойке плаценты. В остальных случаях инфицирование происходит через зараженное материнское молоко. После родов возможно также заражение ребенка контактно-бытовым путем от матери. Тяжесть заболевания у новорожденных зависит от срока беременности, когда произошло инфицирование. Если инфицирование произошло в I или II триместре беременности, вероятность инфицирования составляет до 10%. Если инфицирование имело место в III триместре, то риск передачи инфекции составляет 70%. Если у матери в крови определяется антиген НВsAg, то риск заражения плода равен 20-40 . При дополнительном наличии антигена НBеАg, риск возрастает до 70-90%.
При гепатите В отмечается повышенная частота преждевременных родов и самопроизвольных абортов, число преждевременных родов возрастает втрое. У большинства инфицированных детей острый гепатит В протекает в легкой форме. В подавляющем большинстве случаев (90%) у детей в последующем развивается состояние хронического носительства вируса с риском последующей передачи инфекции. Имеет место также и риск последующего возникновения первичной карциномы или цирроза печени.
Диагностика гепатита В основана на выявлении в крови пациентки различных антигенов и антител к вирусу. При развитии острого гепатита В во время беременности терапия состоит из поддерживающего лечения (диета, коррекция водно-электролитного баланса, постельный режим). При развитии коагулопатии переливается свежезамороженная плазма, криопреципитат. Беременным с различными формами гепатита В следует избегать проведения различных инвазивных процедур во время беременности и в родах. Следует также стремиться к уменьшению продолжительности безводного промежутка и родов в целом.
Наличие гепатита В не является показанием к родоразрешению путем кесарева сечения, так как оно также не исключает вероятности инфицирования (контакт с инфицированной кровью). В послеродовом периоде вакцинации подлежат все новорожденные, родившиеся от матерей — носительниц вируса гепатита В. Новорожденным также показано введение протективного иммуноглобулина «Гепатотект» в первые 12 ч жизни. В случае вакцинации сразу после родов не следует избегать грудного вскармливания. Основным методом профилактики заражения ребенка вирусным гепатитом В является 3-кратное обследование беременных на наличие НВsAg. При риске инфицирования вирусом гепатита В беременной целесообразна 3-кратная вакцинация пациентки рекомбинантной вакциной без риска для ребенка и матери.
Гепатит С характеризуется тенденцией к развитию хронического процесса, ограниченными клиническими симптомами и плохой реакцией на противовирусную терапию. В последствии высока вероятность развития гепатоцеллюлярной карциномы.
Возбудителем гепатита С является РНК-содержащий вирус. Источниками инфекции являются больные с хронической и острой формами гепатита С, а также латентные носители вируса. Вирус передается при трансфузии зараженной крови или ее компонентов. Контактно-бытовой и половой пути заражения являются довольно редкими. Основным путем инфицирования детей является вертикальный путь передачи инфекции от матери. Инкубационный период составляет в среднем 7- 8 нед. Заболевание делится на три фазы: острую, латентную и фазу реактивации. Острая фаза в большинстве наблюдений протекает без клинических проявлений и приблизительно в 60-85% случаев переходит в хроническую форму гепатита с риском развития цирроза печени и гепатоцеллюлярной карциномы.
Острый гепатит С как латентный, так и клинически проявляющийся в 30-50% случаев может закончиться выздоровлением с полной элиминацией НСV. Однако в большинстве случаев он сменяется латентной фазой В период латентной фазы инфицированные лица считают себя здоровыми и никаких жалоб не предъявляют. Фаза реактивации соответствует началу новых клинических проявлений гепатита С с последующим развитием хронического гепатита, цирроза печени и гепатоцеллюлярной карциномы.
Вакцины от гепатита С на сегодняшний день не существует. Всем беременным проводится обязательное скрининговое обследование на гепатит С трижды за беременность. Несмотря на то, что возможна вертикальная передача вируса плоду, гепатит С не является противопоказанием к беременности. Риск заражения плода гепатитом С не зависит от времени заражения матери и составляет около 6%. Передача вируса возможна как во время беременности, так и во время родов.
Нет единого мнения об оптимальном способе родоразрешения беременных с гепатитом С. Некоторые специалисты считают, что кесарево сечение снижает риск инфицирования плода, тогда как другие отрицают это. Преждевременный разрыв плодного пузыря и длительный безводный промежуток увеличивает риск передачи инфекции.
Вирус гепатита С обнаруживается и в грудном материнском молоке, и в этой связи нет также единого мнения о безопасности грудного вскармливания. У всех детей, рожденных от матерей с гепатитом С, в крови также будут отмечаться антитела к вирусу в течение первых 12 мес жизни. Если антитела сохраняются более чем через 18 мес после рождения, то это является подтверждением инфицированности ребенка гепатитом С.
Гепатит D. Возбудителем заболевания является вирус гепатита D, который представляет собой дефектный РНК-содержащий вирус, который способен производить репликацию только с помощью HBsAg-антигена вируса гепатита В. Инфекция передается при трансфузии крови или ее компонентов, а также половым путем. Инфицирование плода происходит вертикальным путем. Диагностика вирусного гепатита D основывается на выявлении антител в сыворотке крови. При инфицировании у новорожденного развивается хронический гепатит D с высоким риском цирроза печени. При гепатите D беременную следует иммунизировать по схеме вакцинации как при гепатите В. Лечение заболевания проводится в рамках общетерапевтических мероприятий.
Гепатит Е. Возбудителем инфекции является РНК-содержащий вирус, который распространяется фекально-оральным путем и вызывает острый гепатит. К плоду вирус попадает путем вертикальной передачи. При гепатите Е повышена частота самопроизвольных выкидышей. Диагноз заболевания основан на прямом выявлении вируса и определении специфических антител. Лечение острого гепатита Е проводят по общим принципам симптоматической терапии.
Гепатит G. Отмечается высокий инфекционный риск для новорожденного при данном заболевании. При наличии гепатита G у беременных в 33% имеется вертикальная передача плоду и новорожденному. Однако у новорожденных до настоящего времени пока ни в одном случае не было выявлено клинических симптомов гепатита. НЕ обнаружено также наличие вируса в молоке, однако по аналогии с гепатитом С целесообразно воздержаться от кормления ребенка грудью. Диагноз устанавливают путем выявления вируса методом ПЦР. Лечение и профилактика острой и хронической форм вирусного гепатита G до сих пор окончательно не разработаны.
Грипп
Грипп, который может протекать у беременных в тяжелой форме, способен приводить к поражению эмбриона и плода. При данном заболевании может происходить самопроизвольное прерывание беременности, гибель плода, аномалии его развития. В результате инфекции возможно рождение недоношенных и функционально незрелых детей, а также детей с недостаточной массой тела.
Влияние вируса гриппа при внутриутробной инфекции обусловлено воздействием возбудителей на плаценту и плод, а также выраженной интоксикацией, повышенной температурой тела, нарушением маточно-плацентарного кровообращения с развитием в последующем гипоксии плода. Во время вспышек гриппа беременных следует иммунизировать поливалентной убитой вакциной.
Дополнительная литература
- Дегтярев Д. Н., Дегтярева М. В., Ковтун И. Ю., Шаламова Л. В.
Принципы диагностики внутриутробных инфекций у новорождённых и тактика ведения детей группы риска. — М.: Перинатология сегодня, 1997. — Т. 3. — С. 18—24. - Володина Н. Н., Дегтярева Д. Н.
Диагностика и лечение внутриутробных инфекций. — М.: Метод. рек. для врачей неонатологов, 1999. - Чебуркин А. В., Чебуркин А. А.
Перинатальная инфекция. — М., 1999. - Н. Н. Володин.
Актуальные проблемы неонатологии. — М.: ГЭОТАР-МЕД, 2004. — 448 с с. - А. Я. Сенчук, З. М. Дубоссарская.
Перинатальные инфекции: практич. пособие. — М.: МИА, 2004. — 448 с с.
Тактика ведения беременности при выявлении ВУИ
В I триместре показано:
- обследование женщины на возможных возбудителей инфекции;
- обследование партнера на инфекции, передающиеся половым путем.
После выявления возбудителя решается вопрос о сохранении беременности. Прерывание рекомендуется при обнаружении краснухи, токсоплазмоза и при первичном инфицировании вирусом герпеса и ЦМВ. В остальных ситуациях возможно сохранение беременности.
Лечение выявленной инфекции в I триместре обычно не проводится. Исключение составляют заболевания, для которых разработаны безопасные препараты:
- кандидозная инфекция;
- бактериальный вагиноз;
- вирус простого герпеса (при реактивации инфекции);
- трихомониаз.
Во II и III триместре рекомендовано лечение тех инфекций, терапия которых на ранних сроках невозможна. Обязательно проводится восстановление микрофлоры влагалища.
Контрольное ультразвуковое исследование и оценка состояния плода выполняются в скрининговые сроки:
- 12-14 недель;
- 18-21 неделя;
- 32-34 недели.
При выявлении пороков развития, несовместимых с жизнью, показано прерывание беременности (на сроке до 22 недель). При сохранении плода проводится терапия, направленная на улучшение плацентарного кровотока и снижение тонуса матки.
Роды при выявленной внутриутробной инфекции могут идти через естественные родовые пути. Рекомендуется избегать любых акушерских операций и вмешательств, повреждающих кожу плода. Кесарево сечение показано при ухудшении состояния ребенка, а также при некоторых формах герпетической и ВИЧ-инфекции.
Симптомы и последствия
Ниже перечислены признаки, которые указывают на инфекцию у беременной:
- кашель, одышка
- сыпь
- лимфоузлы болезненны и увеличены
- высокая температура
- болезненность и припухлость суставов
- насморк, слезотечение, конъюнктивит
- боль в груди
Но эти симптомы в некоторых случаях указывают на аллергическую реакцию. Если это так, то нет риска внутриутробной инфекции малыша. В любом случае, при появлении одного и больше из выше перечисленных признаков нужно идти на очную консультацию к врачу.
ЦМВ (цитомегаловирус)
ЦМВ (цитомегаловирус) относится к группе герпесовирусов. Им заражаются при половых контактах, при тесных бытовых контактах, а также через кровь (если была сделана операция грязными инструментами или переливание от больного донора). Если имело место первичное заражение беременной, то вирус попадает в плаценту, а оттуда к малышу. У ребенка может не быть последствий, что и бывает в большинстве случаев. Но 10 из 100 детей, у которых были больные матери, рождаются с симптоматикой ВУИ.
Последствиями внутриутробного заражения ЦВМ могут стать выкидыши и мертворождения, а также:
- нейросенсорная тугоухость
- недовес при рождении
- гидроцефалия
- микроцефалия
- пневмония
- гепатоспленомегалия
- задержка психомоторного развития
- слепота различных степеней
Если имело место тяжелое сочетанное поражение, 1/3 новорожденных умирают в первые 2-3 месяца после родов. Также очень вероятны такие отдаленные последствия как умственная отсталость, слепота и глухота. Если заражение легкое, то последствия мене серьезные. На сегодня нет лекарства, которое бы помогло при проявлениях цитомегаловируса у недавно рожденных детей. При заражении беременной ЦВМ беременность не прерывают, потому что у ребенка может и не быть симптомов. Врачи прописывают для беременной лечение, чтобы минимизировать развитие осложнений.
ВПГ (вирус простого герпеса)
Врожденная герпетическая инфекция развивается, если у беременной был ВПГ, особенно 2 тип (который передается половым путем). Симптомы появляются в первый месяц после рождения. В основном ВУИ происходит при первичном инфицировании беременной. Ребенок подхватывает инфекцию в большинстве случаев при родах, когда проходит через родовые пути. Но возможность передачи возбудителя болезни через плаценту также нужно учитывать.
Последствия герпеса для ребенка:
- вялость, плохой аппетит
- выкидыш, мертворождение
- характерные высыпания на коже
- лихорадка
- нарушение свертываемости крови
- желтуха
- поражение мозга
- поражение глаз
- пневмония
Тяжелый врожденный герпес чреват инвалидизацией ребенка:
- вегетативное состояние
- олигофрения
- ДЦП
Краснуха
Краснуха очень опасна для эмбриона! Она вызывает различные уродства. Самый высокий риск приходится на беременность до 16-й недели. Последствия ВУИ возбудителем данной болезни:
- микроцефалия
- маловесность при рождении
- выкидыш, мертворождение
- пороки сердца
- глухота (в половине случаев ВУИ)
- катаракта
- поражение кожи
- пневмония
- гепатоспленомегалия
- менингит и энцефалит
Парвовирус В19
Это возбудитель инфекционной эпитемы. У взрослых в основном он незамеченный, потому что протекает латентно. Если беременная заражена им, то она может родить мертвого ребенка, есть риск выкидыша или внутриутробного заражения эмбриона. Дети умирают в 2,5-10 случаях из 100. Особенно опасно заразиться им на 13-28-й неделе гестации.
Последствия для ребенка при ВУИ:
- отеки
- анемия
- поражение мозга
- перитонит
- гепатит
- миокардит
Ветряная оспа
Если больная заразилась ветрянкой, это очень опасно для плода. Если беременная заразилась, а ей в скором времени срок рожать, то есть риск, что ее ребенок умрет. Плод заражается в 25 случаях из 100, но симптомы проявляются не всегда.
Врожденная ветрянка у малышей имеет такие признаки:
- повреждение мозга
- атрофия зрительного нерва, недоразвитие глаз
- недоразвитие конечностей
- сыпь, рубцы зигзагообразной формы
- пневмония
Новорожденных при ВУИ ветрянкой не лечат, потому что симптоматика не прогрессирует. Если мать заразилась за 5 суток до дня родов и позже, врачи могут советовать ввести новорожденному иммуноглобулин, потому что ему не передались антитела от матери.
Гепатит В
Вирус гепатита В передается в основном при незащищенных половых контактах с больным человеком. Он попадает к плоду через плаценту («детское место»). Для беременной очень опасно заразиться с 4-го по 9-й месяц гестации. Последствия ВУИ:
- гепатит В с последующим выздоровлением
- рак печени
- носительство и хроническая форма гепатита типа В
- острая форма гепатита (развивается печеночная недостаточность, ребенок умирает)
- задержка психомоторного развития
- нехватка кислорода
- маловесность
- выкидыш, мертворождение
ВИЧ-инфекция
Вирус иммунодефицита человека (ВИЧ) поражает особые иммунные лимфоциты. Заражение происходит в основном половым путем. Ребенок заражается, прибывая в утробе матери, или проходя при рождении через инфицированные половые пути роженицы. Если не лечить ребенка с врожденной формой ВИЧ, он не выживет даже двух лет, потому что вирус быстро прогрессирует в слабом организме. Смерть происходит от инфекций, которые у здоровых детей не могут привести к летальному исходу.
Чтобы обнаружить ВИЧ у новорожденного, в основном применяется ПЦР. В первые 3-6 месяцев после рождения нет смысла делать анализ на антитела. Важно обнаруживаться ВИЧ у тех, кто ждет ребенка. Им весь срок дают антиретровирусные лекарства, то есть в основном с 4-й недели гестации дается зидовудин. Они не должны кормить грудью своег7о новорожденного. Это в разы повышает шансы здоровья малыша.
Листериоз
Эта болезнь вызывается бактерией листерией. Она может проникать к эмбриону через плаценту, чего не могут многие бактерии. Пути заражения описаны выше. У беременной проявлений болезни может и не быть. В части случаев присутствуют:
- высокая температура
- понос
- рвота
- симптомы, похожие на таковые при гриппе
Последствия заражения плода:
- множественные гнойные очаги, сыпь
- сепсис
- менингит
- лихорадка
- отказ от еды
- мертворождение, спонтанный аборт
Если симптоматика проявилась в первые 7 дней после родов, то дети умирают в 60 случаях из 100. Потому, если у беременной точный диагноз листериоза, ей на 2 недели приписывают ампициллин. ВУИ также лечится, если ребенок действительно заразился от матери.
Сифилис
Первичный сифилис у беременных, который не лечили, передается почти в 100 случаях из 100. Из 10 детей погибают при этом 6, у других обнаруживается врожденная форма болезни. У больной беременной сначала образуется первичная язва, а потом болезнь переходит в латентную форму, время от времени обостряясь.
Заражение эмбриона происходит, даже если у матери болезнь протекает в скрытой форме, с 4-й недели гестации. Последствия ВУИ такие:
- глухота задержка психического развития
- поражение глаз, ушей, рук, ног, зубов
- трещины на коже
- высыпания на кожных покровах
- анемия, желтуха у малыша
- преждевременные роды или рождение мертвого плода
Токсоплазмоз
Передается человеку в основном от кошек, но может передаваться и от других животных. Заразиться беременная может, когда убирает за питомцем или кушает недостаточно термически обработанное мясо, грязные овощи. К моменту беременности большинство женщин уже болели этой болезнью, потому ребенку она не передастся.
При первичном заражении в период беременности в 50 случаях из 100 возбудитель преодолевает плацентарный барьер, заражая эмбрион. Последствия ВУИ для младенца:
- гидро-, микроцефалия
- поражение глаз
- желтуха, увеличение печени и селезенки
- энцефалит, менингит, судороги
- мертворождение, выкидыш
- задержка психомоторного развития