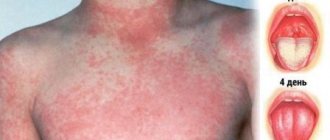
Патогенез
Важно знать! Новинка, которую советуют врачи-эндокринологи для Постоянного контроля Диабета! Нужно всего лишь каждый день… Читать далее >>
Самый простой способ для организма удовлетворить свои потребности в энергии – расщепление глюкозы. В небольшом количестве она всегда находится в нашей крови, ее основным источником является вся пища с углеводами. После еды в крови быстро растет уровень глюкозы, а затем она так же оперативно разносится кровотоком по всем клеткам тела.
Если человек вовремя не поел, дефицит глюкозы покрывается запасом гликогена. Это полисахарид, который хранится в печени и мышцах. Мышечная ткань может запасти до 400 г гликогена. Этот сахар расходуется только локально, по месту нахождения, и не способен попасть в кровь. В печени гликогена меньше – около 100 г у взрослых и 50 г у детей младшего школьного возраста. Он выбрасывается в кровь и разносится по всему телу. В обычных условиях этого гликогена хватает примерно на сутки, при физической нагрузке он тратится меньше, чем за час. У детей гликоген расходуется быстрее, так как их образ жизни активнее, чем у взрослых, а запасов полисахарида меньше.
Причины
Первичный ацетонемический синдром наблюдается у детей, обладающим нервно-артрическим видом телосложением. Факторами, вызывающими данный вид патологии являются:
- наличие сильного испуга;
- сильное физическое напряжение сверх меры;
- эмоциональная нестабильность;
- болевые эффекты;
- стрессовые ситуации;
- избыток жиров и белков в рационе ребёнка и недостаток углеводов.
Вторичный ацетонемический синдром возникает на фоне заболеваний:
- сахарный диабет;
- черепно-мозговая травма;
- на фоне голодания;
- при большом количестве гормонов, выделяемых щитовидной железой;
- токсикоз, появившийся в результате инфекции;
- наличие токсинов в печени;
- разрушение эритроцитов в крови.
Диабет и скачки давления останутся в прошлом
Диабет — причина почти 80% от всех инсультов и ампутаций. 7 из 10 человек умирают из-за закупорки артерий сердца или мозга. Практически во всех случаях причина такого страшного конца одна — высокий сахар в крови.
Сбивать сахар можно и нужно, иначе никак. Но это никак не лечит саму болезнь, а лишь помогает бороться со следствием, а не с причиной болезни.
Единственное лекарство, которое официально рекомендуется для лечения диабета и оно же используется эндокринологами в их работе — это Пластырь от диабета Dzhi Dao.
Эффективность препарата, подсчитанная по стандартной методике (количество выздоровевших к общему числу больных в группе из 100 человек, проходивших курс лечения) составила:
- Нормализация сахара – 95%
- Устранение тромбоза вен – 70%
- Устранение сильного сердцебиения – 90%
- Избавление от повышенного давления – 92%
- Прибавление бодрости днем, улучшение сна ночью – 97%
Производители Dzhi Dao не являются коммерческой организацией и финансируются при поддержке государства. Поэтому сейчас у каждого жителя есть возможность получить препарат со скидкой 50%.
Если кладовая гликогена истощилась, а сахар в кровь так и не поступил, организм включает очередной механизм – липолиз. Это процесс расщепления жиров на жирные кислоты и далее на коэнзим A. В последующих реакциях выделяется нужная организму энергия, синтезируются холестерин и кетоновые тела. В небольших количествах кетоны безопасны, они могут обнаруживаться в моче и крови, не нанося при этом вреда. Если жир расщепляется активно, имеется обезвоживание или проблемы с почками, ацетон не успевает выводиться и начинает копиться. В этом случае говорят об ацетонемическом синдроме. Его признаками являются рост кетонов в крови — ацетонемия и выделение их с мочой – ацетонурия.
Дополнительно: Надо ли бояться ацетона в моче и причины его повышения, об этом мы рассказали здесь — читать подробнее
Дифференциальная диагностика
Главным образом дифференциальная диагностика проводится с диабетическим кетоацидозом. Основные особенности недиабетического кетоацидоза: отсутствие значительной гипергликемии или гипогликемия, отсутствие классического «диабетического» анамнеза и, как правило, значительно лучшее состояние пациента.
Важным является определение первичности или вторичности развившегося недиабетического кетоацидоза. При диагностике вторичного ацетонемического синдрома необходимо обратить определённое внимание на поиск этиологического фактора, поскольку это имеет существенное значение для выбора дальнейшей лечебной тактики.
Причины синдрома
К нехватке глюкозы и ацетонемическому синдрому разной степени выраженности могут привести:
- Недостаточное поступление углеводов с пищей, например, низкоуглеводная диета для похудения или для больных сахарным диабетом. Длительный дефицит углеводов уменьшает способность печени запасать гликоген, поэтому ацетонемический синдром развивается у приверженцев такого питания быстрее, чем у людей, потребляющих достаточное количество сахаридов. У ребенка способность накапливать гликоген формируется еще до рождения. Из-за малого его количества младенцам нужно более частое питание с обязательным содержанием углеводов.
- Жирная, высокобелковая пища при относительной нехватке углеводов.
- Состояния, сопровождающиеся повышенным расходом энергии. Ацетонемический синдром по этой причине характерен для детей до 8 лет. У них стресс, инфекция, отравление и даже пропуск ужина могут привести к образованию кетонов. У части малышей наблюдается предрасположенность к ацетонурии, обычно они худенькие, подвижные, легко возбудимые, с плохим аппетитом и маленьким запасом гликогена. У взрослых ацетон в существенных количествах выделяется после серьезных травм, операций, выхода из комы, поэтому в это время больному вводят глюкозу внутривенно.
- При токсикозе или гестозе, которые сопровождаются рвотой и отсутствием аппетита, беременная женщина недополучает углеводов, поэтому в организме начинают расщепляться жиры, и выделяться ацетон. Как и у детей, причиной синдрома у беременных могут быть любые заболевания и эмоциональные переживания.
- Длительная высокоинтенсивная нагрузка на мышцы сжигает запасы глюкозы и гликогена, причем усвоение глюкозы продолжается еще некоторое время после тренировки или физического труда. Чтобы избежать ацетонемического синдрома, рекомендуют после нагрузки употреблять углеводы – «закрывать углеводное окно». И наоборот, если цель занятия – похудение, после него пару часов есть нежелательно, так как именно в это время расщепляется жир.
- Прекращение выработки инсулина при 1 типе диабета. При отсутствии собственного гормона сахар полностью теряет возможность попасть в клетки, поэтому жиры расщепляются особенно быстро. Ацетонемический синдром развивается при дебюте сахарного диабета или недостаточной дозе назначенных препаратов инсулина и может в краткие сроки перерасти в кетоацидотическую кому.
- Существенное снижение синтеза инсулина при тяжелой стадии 2 типа диабета. Как правило, в это время больного переводят на инсулинотерапию, чтобы предотвратить гипергликемию и голодание тканей. Если этого не происходит, одновременно с ростом сахара крови развивается ацетонемический синдром.
- Сильная инсулинорезистентность у больных с 2 типом диабета. При этом состоянии в крови достаточно и сахара, и инсулина, но мембраны клеток не пропускают их внутрь. Главная причина резистентности – ожирение и недостаток движения.
- Частое употребление алкоголя способствует уменьшению количества гликогена, что ускоряет развитие синдрома.
Клиника, диагностика
В настоящее время НАД рассматривается как энзимодефицитное состояние, характеризующееся:
— повышенной возбудимостью и быстрой истощаемостью нервной системы на всех уровнях рецепции с наличием доминантного очага застойного возбуждения в гипоталамо-диэнцефальной области;
— недостаточностью ферментов печени (глюкозо-6-фосфатазы, гипоксантин-гуанин-фосфорибозилпирофосфатсинтетазы);
— низкой ацетилирующей способностью ацетилкоэнзима А вследствие дефицита щавелевой кислоты, необходимой для вовлечения ацетилкоэнзима А в цикл Кребса;
— нарушением механизма повторного использования мочевой и молочной кислот;
— нарушением жирового и углеводного обмена;
— нарушением эндокринной регуляции метаболизма.
Дети с НАД сразу после рождения отличаются повышенной возбудимостью, эмоциональной лабильностью, нарушением сна, пугливостью. Возможны аэрофагия и пилороспазм. К годовалому возрасту обычно заметно отстают в массе от сверстников. Нервно-психическое развитие, напротив, опережает возрастные нормы. Дети быстро овладевают речью, проявляют любознательность, интерес к окружающему, хорошо запоминают и пересказывают услышанное, однако часто в поведении проявляют упрямство и негативизм. Начиная с 2–3-летнего возраста у них отмечаются эквиваленты подагрических приступов и кризов в виде преходящих ночных болей в суставах, абдоминальных болей спастического характера, дискинезий желчевыводящих путей и желудка, непереносимости запахов, других видов идиосинкразии, мигрени, ацетонемических кризов. Иногда прослеживается стойкий субфебрилитет. Возможны тики, хореические и тикоподобные гиперкинезы, аффективные судороги, логоневроз, энурез. Нередко отмечаются респираторные и кожные аллергические проявления в виде атопической бронхиальной астмы, атопического дерматита, крапивницы, отека Квинке, причем в возрасте до 1 года аллергические поражения кожи крайне редки и проявляются, как правило, после 2–3 лет. В патогенезе кожного синдрома имеют значение не только аллергические, но и парааллергические (неиммунные) реакции, обусловленные высвобождением биологически активных веществ, уменьшением синтеза циклических нуклеотидов и мощным ингибирующим действием мочевой кислоты на аденилциклазу. Одним из типичных проявлений НАД является салурия с преимущественной уратурией. Выделение солей периодически наблюдается одновременно с дизурией, не связанной с инфекцией. Однако возможно развитие пиелонефрита, который часто присоединяется при нефролитиазе. У детей препубертатного и пубертатного возраста часто выявляется астеноневротический или психастенический тип акцентуации. У девочек проявляются истероидные черты характера. Среди неврозов преобладает неврастения. Вегетососудистая дисфункция чаще протекает по гиперкинетическому типу.
Наиболее выраженным проявлением обменных нарушений у детей с НАД, требующим интенсивной врачебной помощи, является ацетонемический криз. Его развитию может способствовать множество факторов, которые в условиях повышенной возбудимости нервной системы воздействуют стрессогенно: испуг, боль, конфликт, гиперинсоляция, физическое или психоэмоциональное напряжение, смена микросоциальной среды, пищевые погрешности (большое содержание белков и жиров) и даже положительные эмоции «в избытке». Повышенная возбудимость вегетативных центров гипоталамуса, которая имеет место при НАД, под действием стрессогенных факторов вызывает усиленный липолиз и кетогенез, вследствие чего образуется большое количество кетоновых тел. При этом возникает раздражение рвотного центра ствола головного мозга, которое вызывает рвоту.
Ацетонемические кризы возникают внезапно или после предвестников (ауры), к которым можно отнести анорексию, вялость, возбуждение, мигренеподобную головную боль, тошноту, абдоминальные боли преимущественно в околопупочной области, ахоличный стул, запах ацетона изо рта.
Клиническая картина ацетонемического криза:
— многократная или неукротимая рвота в течение 1–5 дней (попытка напоить или покормить ребенка провоцирует рвоту);
— дегидратация и интоксикация (бледность кожи с характерным румянцем, гиподинамия, мышечная гипотония);
— беспокойство и возбуждение в начале криза сменяются вялостью, слабостью, сонливостью, в редких случаях возможны симптомы менингизма и судороги;
— гемодинамические нарушения (гиповолемия, ослабление сердечных тонов, тахикардия, аритмия);
— спастический абдоминальный синдром (схваткообразные или упорные боли в животе, тошнота, задержка стула);
— увеличение печени на 1–2 см, сохраняющееся в течение 5–7 дней после купирования криза;
— повышение температуры тела до 37,5–38,5 °С;
— наличие в моче, рвотных массах, выдыхаемом воздухе ацетона, в крови — повышенной концентрации кетоновых тел;
— гипохлоремия, метаболический ацидоз, гипогликемия, гиперхолестеринемия, бета-липопротеинемия;
— в периферической крови умеренный лейкоцитоз, нейтрофилез, умеренное повышение СОЭ.
Симптомы ацетонемии
Первые симптомы связаны с интоксикацией организма кетонами. Может ощущаться вялость, утомляемость, тошнота, головная боль, тяжесть или другие неприятные ощущения в животе.
По мере нарастания концентрации кетонов наблюдаются:
- упорная рвота. Приступы могут продолжаться несколько часов, за это время больной теряет всю жидкость, потребляемую за это период. От рвотных масс исходит запах ацетона. Возможна рвота желчью и даже кровью;
- такой же запах ощущается и от дыхания больного, а иногда и от его кожи;
- боль в брюшине, часто похожая на симптомы острого живота: резкая, усиливающаяся после надавливания. Возможна диарея;
- быстро нарастающая слабость. Ребенок лежит и вяло реагирует на интересные ему ранее вещи;
- светобоязнь – больной просит выключить свет, задернуть шторы, жалуется на резь в глазах;
- может подниматься температура;
- обезвоживание из-за частой рвоты и диареи, у больного сухие губы, мало слюны, моча выделяется в небольшом объеме, темного цвета.
Если ребенок склонен к ацетонемическому синдрому, у него от раза к разу повторяются одинаковые симптомы. Уже через пару эпизодов ацетонемии родители учатся быстро распознавать и купировать это состояние. Лечение в домашних условиях возможно при начальных проявлениях синдрома. Если малыш мало пьет и стал реже мочиться, так как вся жидкость выходит с рвотой, нужно вызывать врача. Чем младше ребенок, тем быстрее у него развивается обезвоживание.
Как лечить?
Терапевтические мероприятия, направленные на устранение причин и симптомов ацетонемии делятся на 2 этапа: купирование ацетонемического криза (осуществляется в период приступов) и терапия в перерывах между приступами.
Купирование криза
Обильная рвота приводит к тяжелым последствиям, связанным с нарушением обмена веществ, потерей жидкости, что негативно сказывается на состоянии всех органов и систем ребенка. Следовательно, приступы рвоты необходимо предотвращать и подавлять.
В период приступов необходимо следить за тем, чтобы ребенок потреблял достаточное количество жидкости, что позволит восстановить нормальный водный баланс организма, вывести токсины и шлаки.
Пить необходимо часто, но небольшими порциями, чтобы не спровоцировать новые приступы рвоты.
Для отпаивания хорошо подходит раствор Регидрон, травяные чаи, витаминные морсы, минеральная негазированная вода.
Пациенту в условиях стационара назначают инфузионную терапию (введение растворов при помощи капельницы). Инфузионная терапия направлена на:
- Устранения дефицита жидкости в организме, детоксикацию, улучшение обменных процессов и микроциркуляции.
- Восстановление нормального кислотно – щелочного баланса организма.
- Снабжение организма легкоусваиваемыми углеводами, для поддержания жизненных сил.
Лечение в периоды между приступами
Для нормализации состояния ребенка, устранения причин и последствий недуга ребенку необходимо:
- Принимать ферментные препараты, улучшающие процесс переваривания пищи, восстанавливающие нормальный метаболизм.
- Соблюдение диеты.
- Прием противовирусных препаратов и антибиотиков (осуществляется строго по назначению врача).
- Прием обезболивающих средств (если пациент жалуется на боли в животе).
- Очищающие клизмы для детоксикации организма.
О симптомах и лечении артрита у детей узнайте из нашей статьи.
Опасность и возможные последствия
Чаще всего кетоновые тела образуются в небольшом объеме, выводятся почками и легкими и не связаны с риском для здоровья. Ацетонемический синдром представляет опасность только для детей, ослабленных больных и диабетиков.
У малышей из-за маленького веса быстро поднимается концентрация кетонов, начинается рвота и развивается опасное обезвоживание. В таком состоянии им невозможно дать углеводы в пище, поэтому требуется госпитализация и внутривенные вливания глюкозы.
При сахарном диабете ацетон безопасен, если его причиной стала низкоуглеводная диета или физическая работа. А вот если ацетонемический синдром сопровождается высоким сахаром крови, риск существенно возрастает. В этом состоянии наблюдается полиурия – избыточное выделение мочи, которое вызывает дегидратацию. На недостаток жидкости организм реагирует задержкой мочи, а следовательно, и кетонов. К накоплению ацетона может привести и диабетическая нефропатия, сопровождающаяся почечной недостаточностью. Рост концентрации кетонов увеличивает плотность крови и ее кислотность. Комплекс вышеперечисленных нарушений называют диабетическим кетоацидозом. Если вовремя его не купировать, кетоацидоз приводит к гипергликемической коме.
Этиология и патогенез
Главным фактором, на фоне которого возникает АС, является аномалия конституции — нервно-артритический диатез (НАД). Однако любые стрессогенные, токсические, алиментарные, эндокринные влияния на энергетический обмен, даже у детей без НАД, могут вызывать развитие ацетонемической рвоты.
В норме катаболические пути углеводного, белкового и жирового обменов пересекаются в цикле Кребса — универсальном пути энергообеспечения организма.
Пусковым фактором развития кетоза является стресс с относительным преимуществом контринсулярных гормонов и алиментарные нарушения в виде голодания или чрезмерного потребления жирной и белковой пищи (кетогенных аминокислот) при недостатке углеводов. Абсолютный или относительный недостаток углеводов служит причиной стимуляции липолиза для обеспечения потребностей организма.
Кетоз вызывает ряд неблагоприятных последствий для организма ребенка. Во-первых, при значительном повышении уровня кетоновых тел, являющихся донаторами анионов, возникает метаболический ацидоз с увеличенным анионным интервалом — кетоацидоз.
Его компенсация осуществляется за счет гипервентиляции, которая приводит к гипокапнии, вызывающей вазоконстрикцию, в том числе и церебральных сосудов. Во-вторых, излишек кетоновых тел оказывает наркотическое влияние на центральную нервную систему, вплоть до развития комы. В-третьих, ацетон является жирорастворителем и повреждает липидный бислой клеточных мембран.
Кроме того, для утилизации кетоновых тел необходимо дополнительное количество кислорода, что может вызывать несоответствие между доставкой и потреблением кислорода, то есть способствует развитию и поддержанию патологического состояния.
Излишек кетоновых тел раздражает слизистую оболочку желудочно-кишечного тракта, что клинически манифестирует рвотой и абдоминальным болевым синдромом. Перечисленные неблагоприятные эффекты кетоза в сочетании с другими расстройствами водно-электролитного и кислотно-основного равновесия (гипо-, изо- и гипертоническое обезвоживание, метаболический ацидоз вследствие потерь бикарбоната и/или накопления лактата) способствуют более тяжелому течению заболевания, увеличивают продолжительность пребывания в отделении интенсивной терапии.
НАД — это полигенно наследуемая аномалия обмена веществ, в основе которой лежат нарушение пуринового обмена с избыточной продукцией мочевой кислоты и ее предшественников, нестойкость других видов обмена (в первую очередь углеводного и липидного) со склонностью к кетозу и медиаторных функций нервной системы, определяющих особенности ее реакции.
К генетическим факторам, вызывающим гиперурикемию, относится ряд энзимных дефектов: дефицит гипоксинтингуанилфосфорибозилтрансферазы; дефицит глюкозо-6-фосфатазы; повышение каталитической активности фермента фосфорибозил-пирофосфатсинтетазы.
Наследственный фактор нарушений пуринового обмена подтверждается результатами семейно-генетических исследований детей с НАД: частота выявления нервно-психических заболеваний в родословной таких детей составляет до 18 %, подагра регистрируется в 22 % случаев. У родственников 1-й степени родства — мочекаменная болезнь, мочекислый диатез, обменные артриты встречаются в 20 раз чаще, чем в контрольной группе. В 2 раза чаще отмечаются заболевания системы кровообращения (ишемическая болезнь сердца, гипертоническая болезнь), сахарный диабет.
Свободные пурины и образующие их соединения имеют особое значение в жизнедеятельности организма; синтез пуриновых оснований является центральным звеном биосинтеза нуклеотидов, которые принимают участие почти во всех внутриклеточных биохимических процессах:
— они являются активированными предшественниками ДНК и РНК;
— производные нуклеотидов — активированные промежуточные продукты многих синтетических реакций;
— адениннуклеотид аденозинтрифосфорной кислоты — универсальная энергетическая «валюта» в биологических системах;
— адениннуклеотиды — компоненты трех основных коферментов: НАД, ФАД и СОА;
— пуриновые нуклеотиды играют общерегулирующую роль в биологической активности клеток, превращаясь в циклические нуклеотиды — циклический аденозинмонофосфат и циклический гуанозинмонофосфат.
У человека основными источниками синтеза пуринов являются фосфорибозилмонофосфат и глутамин, из которых образуется инозиновая кислота — основной предшественник пуриновых нуклеотидов, содержащий полностью готовую пуриновую кольцевую систему.
Из года в год возрастает интерес к изучению пуринового обмена и его конечного продукта — мочевой кислоты, что связано с неуклонным увеличением частоты как бессимптомной, так и клинически манифестной гиперурикемии — биологической аномалии, свойственной только человеку.
Выделяют три основных пути образования мочевой кислоты в организме:
— из пуринов, которые высвобождаются при тканевом распаде;
— из пуринов, содержащихся в пище;
— из синтетически созданных пуринов.
Гиперурикемию можно выявить почти у 38 % людей, причем уровень мочевой кислоты в крови зависит от возраста, пола, национальности, географической зоны, уровня урбанизации, типа питания.
Гиперурикемия бывает первичной и вторичной. Существуют два пути развития первичной гиперурикемии — метаболический и выводящий. Первый связан со значительным поступлением пуринов в организм и усиленным их образованием. Повышенный синтез мочевой кислоты, характерный для НАД, может быть обусловлен различными ферментными дефектами, основными из которых являются:
— недостаток глутаминазы, трансформирующей глутамин в глутаминовую кислоту и аммиак;
— дефицит гипоксинтингуанилфосфорибозилтрансферазы, обеспечивающей синтез пуриновых оснований (гипоксантина и гуанина) и нуклеотидов (инозинмонофосфата и гуанозинмонофосфата);
— гипопродукция уриказы, превращающей мочевую кислоту в более разведенный алантоин;
— избыток фосфорибозилпирофосфатсинтетазы, которая катализирует процесс синтеза фосфорибозилпирофосфата из АТФ и рибозо-5-фосфата;
— гиперактивность ксантиноксидазы, окисляющей гипоксантин в ксантин и мочевую кислоту.
Диагностика
Определить причину плохого самочувствия у больного диабетом обычно не составляет труда, если он регулярно пользуется глюкометром и следит за своим здоровьем. Диагностировать первое появление ацетонемического синдрома у ребенка бывает сложнее, обычно малышей с характерными симптомами госпитализируют в инфекционное отделение, а после установки правильного диагноза переводят для лечения в гастроэнтерологическое. В дальнейшем родители могут приобрести средства для определения ацетона в домашних условиях, и вовремя диагностировать и купировать синдром без помощи врачей.
Лабораторные методы
В стационаре для выявления кетонов производят забор крови и мочи. В моче ацетон определяется полуколичественным методом, результат такого анализа – от 1 до 4 плюсиков. Чем выше концентрация, тем плюсов больше.
Расшифровка анализа:
| Результат | Степень тяжести состояния |
| + | Легкая степень, лечение ацетонемического синдрома может проводиться дома. |
| ++ | Средняя степень. Если синдром до этого возникал неоднократно, известны особенности его протекания и методы лечения, с кетонами можно справиться самостоятельно. Если ацетонемический синдром возник впервые, требуется наблюдение врача. |
| +++ | Критическое повышение, кетонов в 400 раз больше нормы, необходима госпитализация. |
| ++++ | Тяжелое состояние, ацетон превышает норму в 600 раз, без лечения возможно развитие кетоацидоза. |
Кетоны крови определяются в ммоль/л, норма – при от 0,4 до 1,7 в зависимости от используемого при анализе метода. Повышение до 100-170 ммоль/л наблюдается кетоацидотической коме.
Экспресс-методы
В домашних условиях ацетон в моче легко выявляется специальными тест-полосками, которые действуют по принципу лакмусовой бумаги. Самые распространенные – Кетоглюк (50 шт за 240 руб), Урикет (150 руб), Кетофан (200 руб). Концентрация кетонов определяется по степени окрашивания тест-полоски после погружения ее в мочу.
Правила использования:
- Собрать мочу в контейнер. Для анализа моча должна быть свежей, хранить больше 2 часов ее нельзя.
- Достать тест-полоску. Тут же закрыть контейнер, так как от соприкосновения с воздухом оставшиеся полоски портятся.
- Опустить часть полоски с индикатором в мочу на 5 секунд.
- Вынуть полоску. Прикоснуться ее ребром к салфетке, чтобы впиталась лишняя моча.
- Через 2 минуты сравнить окраску индикатора со шкалой на упаковке и определить уровень кетонов. Чем насыщеннее цвет, тем ацетон выше.
Больные сахарным диабетом могут пользоваться моделями глюкометров, которые способны определять и сахар, и кетоны крови. Для выявления ацетона придется приобрести отдельные полоски.
Диагностика заболевания
Важным диагностическим методом является оценка клинической картины недуга. Так, о наличии ацетонемии можно говорить в том случае, когда:
- приступы рвоты повторяются многократно;
- приступы имеют большую продолжительность по времени;
- повторяются не менее 2 раз в неделю;
- чередуются с периодами ремиссии, когда пациент чувствует себя нормально;
- приступы имеют одинаковое течение (индивидуальное для каждого пациента);
- возникают и затухают спонтанно.
Для постановки точного диагноза необходимо провести ряд лабораторных исследований:
- Анализ крови (оцениваются количественные показатели глюкозы, лейкоцитов, нейтрофилов, а также СОЭ).
- Анализ мочи для определения уровня содержания кетоновых тел (количество обозначается знаком +, показатели могут варьироваться от + до ++++).
- Электролитное исследование для определения степени обезвоженности организма, выявления, какую именно воду (соленую или несоленую) он преимущественно теряет.
Купирование ацетонемического синдрома
Общее правило лечения ацетонемического синдрома – устранение обезвоживания. Больному нужно часто, но понемногу давать жидкость. Если наблюдается многократная рвота, поить придется буквально по ложке каждые 5 минут до тех пор, пока не исчезнут симптомы дегидратации и не начнет в нормальном количестве выделяться моча. Одновременно нужно устранить причину ацетонемии.
У больных диабетом
Если ацетон появляется при сахарном диабете, первым делом нужно измерить глюкозу крови. Если она существенно повышена (> 13 ммоль/л), велик риск кетоацидоза. Чтобы снизить глюкозу, нужно выпить Метформин, исключить из диеты углеводы или сделать корректирующую подколку инсулина.
Ацетон начнет снижаться только после того, как восстановится нормальное мочеиспускание. Для этого необходимо обильное несладкое питье, лучше всего обычная негазированная вода комнатной температуры. При длительной рвоте применяют специальные регидрационные растворы – Регидрон, Трисоль, Гидровит. Пища и напитки с углеводами разрешены только после нормализации гликемии.
Если при диабете наблюдается заторможенность больного и необычное дыхание, нужно вызвать скорую помощь. Такие симптомы характерны для прекоматозного состояния, справиться с ним дома не получится.
В стационаре больному снизят сахар крови при помощи инсулинотерапии, капельницами восстановят объем жидкости в теле. При своевременном обращении к медикам ацетонемический синдром не приносит существенного вреда организму.
У детей
Ацетонемический синдром – нередкое явление у детей, чаще всего его можно быстро купировать. Некоторые малыши «выдают» ацетон на каждое недомогание, например, простуду или однократную рвоту, и даже на новые для них ситуации или слишком активные игры. Бояться этого не стоит, к подростковому возрасту запасы гликогена увеличатся, и синдром больше не будет беспокоить.
Дополнительно: Пахнет ацетоном изо рта — что это значит и в чем опасность?
Как только у ребенка будет замечено необычное состояние – плаксивость, вялость, сонливость, нужно тут же измерить ацетон в моче. Для этого всегда дома должны быть тест-полоски. Если имеется даже небольшое повышение, значит, присутствует нехватка углеводов. Быстрее всего ее можно восполнить при помощи сладкого питья: компота, сока, чая. После такого лечения образование кетонов прекращается, рвоты не будет.
Часто ацетонемический синдром не удается предотвратить в самом начале. Бывает, что рвота у ребенка начинается рано утром, после ночного сна. В этом случае тактика та же самая – поим малыша. Лучше использовать компот из сухофруктов, раствор глюкозы или лимон с медом. Питье обязательно должно быть теплым. Газированные напитки нежелательны, так как могут усилить боль в животе. Если рвота повторяется, даем жидкость очень часто, по чайной ложке. Если у ребенка диабет, но гипергликемия отсутствует, сладкое питье должно сопровождаться введением инсулина.
Во время лечения нужно следить за наличием мочеиспусканий. При достаточном употреблении жидкости ребенок должен ходить в туалет хотя бы раз в 3 часа, моча должна быть светлой.
Вызывать скорую помощь при ацетонемическом синдроме у детей нужно в следующих случаях:
- младенцу меньше 4 месяцев;
- рвота, несмотря на лечение, становится тяжелее, теряется вся выпитая жидкость;
- мочи нет больше 6 часов;
- рвотные массы содержат мелкие частички темно-коричневого цвета;
- наблюдается спутанное сознание или неадекватное поведение;
- присутствует необычное дыхание;
- боль в животе не проходит после приступа рвоты.
После первого появления синдрома нужно обратиться к педиатру для установления его причины. Для исключения проблем с усвоением углеводов он назначит общие анализы крови и мочи, исследование на сахар.
Диагностика[править | править код]
Опирается на данные анамнеза, анализировании жалоб, клинической симптоматики и результатов дополнительных инструментальных и лабораторных исследований.
Диагностические критерии:
- повторяющиеся тяжёлые упорные эпизоды рвоты;
- межприступный период различной продолжительности между эпизодами рвоты;
- продолжительность эпизодов рвоты от нескольких часов до суток;
- отрицательные результаты обследования, которые бы могли связать этиологию рвоты с проявлениями патологии со стороны органов ЖКТ;
- приступы рвоты характеризуются стереотипией — каждый эпизод аналогичен предыдущему по времени, интенсивности и продолжительности;
- в некоторых случаях приступы рвоты могут заканчиваться спонтанно и без лечения;
- сопутствующие симптомы включают тошноту, боль в животе, головную боль, адинамию, фотофобию, заторможенность;
- рвоте сопутствуют лихорадка, бледность, диарея, дегидратация, избыточная саливация и социальная дезадаптация;
- рвотные массы часто содержат желчь (76 %), слизь (72 %) и кровь (32 %) в результате ретроградного пролабирования кардиальной части желудка сквозь гастроэзофагальный жом (пропульсивная гастропатия).
В случаях, когда ацетонемическая рвота развивается на фоне известных провоцирующих факторов (инфекция, периоперационное голодание, опухоли ЦНС и так далее) диагностируется вторичный недиабетический кетоацидоз.
Лабораторная диагностика[править | править код]
В клиническом анализе крови специфические изменения отсутствуют — картина в первую очередь отражает ту патологию, на фоне которой развился эпизод кетоза.
Наиболее типичным признаком в клиническом анализе мочи является наличие кетонурии от «одного плюса» (+) до «четырёх плюсов» (++++) полуколичественным методом с нитропруссидом. Глюкозурия (наличие глюкозы в моче) не является обязательным симптомом, однако практически всегда появляется на фоне инфузии (внутривенном капельном вливании) растворов глюкозы.
Диагностически значимы результаты биохимического анализа крови: чем дольше продолжается эпизод ацетонемической рвоты, тем выраженнее дегидратация, тем выше показатель гематокрита (соотношение форменных элементов крови к плазме) и показателя общего белка. при значительном обезвоживании определяется увеличение мочевины в крови свыше 8,8 ммоль/л (следствие преренальной олигурии и гемоконцентрации). Чаще наблюдается изотоническое обезвоживание (следствие «сбалансированных» потерь натрия и воды). При выраженном ацидозе калий сыворотки нормальный или повышен. В случаях продолжительной рвоты и незначительно выраженного ацидоза наблюдается гипокалиемия.
При исследовании показателей кислотно-щелочного состояния чаще определяется компенсированный (полная или частичная компенсация ацидоза осуществляется за счёт гипервентиляции) или декомпенсированный метаболический ацидоз с увеличенным анионным интервалом.
Функциональная диагностика[править | править код]
Важным компонентом обследования является эхокардиоскопия с определением показателей центральной гемодинамики — чаще определяются снижение конечного диастолического объёма левого желудочка, снижение центрального венозного давления, умеренное снижение фракции выброса и за счёт этого снижение ударного объёма левого желудочка. Несмотря на эти изменения, сердечный индекс может быть увеличенным за счёт значительной тахикардии.
Литература
- Курило Л. В. Первичный ацетонемический синдром у детей. // Medicus Amicus.— 2002.— № 5 — С. 4-7.
- Казак С., Бекетова Г. Диагностика и диетотерапия ацетонемического синдрома у детей. // Ліли України.— 2005.— № 1 — С. 83-86. (укр.)
- Зайчик А. Ш., Чурилов Л. П. Основы патохимии.— С.-Петербург: Элби-СПб — 2000.— 687 с.
- Лукьянчиков В. С. Кетоз и кетоацидоз. Патобиохимический и клинический аспект. // РМЖ.— 2004.— Том 12.— № 23.
- Гуменюк Н. И., Киркилевский С. И. Инфузионная терапия. Теория и практика.— К.: Книга плюс — 2004.— 208 с.
- Корпачёв В. В. Сахара и сахарозаменители.— К.: Книга плюс — 2004.— 320 с.