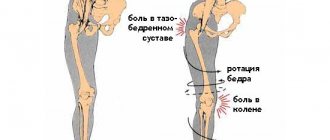
Причины заболевания
Нерв, пролегающий в канале из твердых тканей, надежно защищен от внешних воздействий. Но при этом он может пострадать при деформациях канала, стенки которого его окружают. К деформациям приводит перенапряжение связок и сухожилий, вызывающее временное ухудшение кровоснабжения тканей и дефицит в них питательных веществ. При постоянных нагрузках на этот участок изменения закрепляются и становятся постоянными: ткани туннеля утолщаются, разрыхляются или отекают. Как следствие, в туннеле не остается свободного пространства и возрастает давление на нервный ствол, после чего начинают развиваться нарушения его функций — проведение двигательных сигналов.
Гораздо реже туннельный синдром может быть вызван отеком самого нерва. Это состояние способно развиться по причине общей интоксикации организма солями тяжелых металлов, производными мышьяка и ртути и прочими отравляющими веществами. Продолжительное течение кого-либо заболевания, требующего применения антибиотиков, мочегонных и сосудорасширяющих средств также может привести к развитию туннельной невропатии.
Факторы риска
Туннельный синдром, как правило, развивается в участках, подвергающихся постоянным или регулярным нагрузкам в виде однообразных, повторяющихся движений. Но кроме механического раздражения нерва и окружающих его тканей, к заболеванию могут привести другие факторы.
В группу риска возникновения туннельного синдрома входят следующие категории населения:
- люди, чья профессиональная или повседневная деятельность включает однотипные сгибательно-разгибательные движения (парикмахеры, наборщики текста, теннисисты, сурдопереводчики, музыканты — чаще всего скрипачи, гитаристы, маляры и пр.);
- люди старше 50-ти лет (возрастные изменения, происходящие во всем организме, неизменно касаются и костных тканей);
- люди, страдающие от эндокринных заболеваний (сахарного диабета, дисфункции щитовидной железы, гипофиза), которые значительно нарушают способности тканей к восстановлению;
- люди, имеющие семейную историю заболеваний опорно-двигательного аппарата или страдающие этими заболеваниями (артрит, остеохондроз и пр.);
- люди, часто подвергающиеся микротравмам суставов и связок (грузчики, бодибилдеры, каменщики и пр.);
- люди с аутоиммунными заболеваниями (системной красной волчанкой, ВИЧ и пр.)
Причины
Главная причина, по которой развивается туннельный синдром, это увеличение в объемах синовиальных оболочек, которые окружают сухожилия и оказывают на серединный нерв давление.
Синовиальные оболочки способны вырабатывать секрет, необходимый для уменьшения трения между стенками сухожилий, что облегчает их работу.
Все предрасполагающие факторы, способные провоцировать развитие туннельного синдрома запястья, условно можно разделить на две категории:
Прямые – сюда относят все предпосылки, которые напрямую влияют на ущемление нерва:
- неконтролируемое увеличение массы тела, что способствует росту и увеличению в объемах мышц и сухожилий;
- гормональные заболевания;
- акромегалия – патология передней доли гипофиза, при которой отмечается неконтролируемый рост костной ткани, что сопровождается утолщением и расширением кистей рук;
- наследственная предрасположенность;
- возраст после 55 лет;
- задержка жидкости в организме, при которой вся попадаемая в организм вода не выводится почками, а накапливается в тканях, провоцируя отеки;
- новообразования (кисты) в области запястья, которые стремительно увеличиваются в размерах и давят на нерв;
- ревматоидный артрит, артроз, хронические воспалительные процессы в мышцах и сухожилиях;
- тендовагинит – болезнь, при которой воспалительный процесс поражает сухожилия, провоцируя их отечность и рыхлость.
Косвенные – в эту группу относят те факторы, которые могут ускорять развитие заболевания, а также усугублять его течение, в случае, когда у человека имеются хронические заболевания.
Сюда относят следующие частые факторы риска развития болезни:
- наличие вредных привычек, особенно хронический алкоголизм;
- частый травматизм области запястья (переломы, разрывы сухожилий, защемления);
- длительная механическая работа кистями рук: компьютерная верстка, работа за станком, игра на музыкальных клавишных инструментах, вышивание и кройка одежды.
В группу риска попадают люди в возрасте после 45 лет, когда на фоне гормональных изменений может резко увеличиваться вес, а также развиваться системные заболевания, такие как артрит, артроз, подагра.
Виды туннельного синдрома
Синдром запястного канала — наиболее распространенный вид туннельной невропатии и очень часто — принимаемый за единственную форму заболевания.
Но это состояние может развиться при ущемлении следующих нервных стволов:
- надлопаточного нерва — синдром надлопаточной выемки (чаще всего встречается у легкоатлетов, занимающихся метанием ядра и копья, у теннисистов, волейболистов — синдром развивается на «рабочей» стороне тела);
- локтевого нерва;
- срединного ладонного нерва;
- лучевого нерва;
- срединного запястного нерва;
- малоберцового нерва;
- большеберцового нерва;
- пальцевого подошвенного нерва.
Сдавливание любого из перечисленных нервов относится к категории туннельных синдромов и имеет схожие симптомы.
Общие сведения
Заболевание вызвано раздражением или повреждением срединного нерва руки, когда в области запястья на него постоянно действует высокое давление.
Каждая рука снабжена тремя нервами, которые отвечают, как за движения (двигательные волокна), так и за ощущения, чувствительность данной области (сенсорные волокна). Срединный нерв обеспечивает движение и чувствительность внутренней части руки и мышц, обеспечивающих движение большого пальца.
Туннельный синдром запястного канала
Срединный нерв тянется от плеча и предплечья к кисти. На внутренней стороне запястья он проходит через так называемый кистевой туннель. Этот проход образован костями запястья и стабилизирующей связкой. В дополнение к нерву, сухожилия мышц, сгибающих пальцы, также проходят через кистевой туннель.
Синдром карпального канала встречается в различных формах. В легких случаях отмечается только слабый дискомфорт, в тяжелой форме возможно развитие постоянного паралича.
Некоторые люди словно «предназначены» для туннельного синдрома, потому что у них узкий запястный канал обусловлен анатомически, с рождения. Если одно и то же движение осуществляется долго или напрягает запястье во время работы, синдром запястного канала развивается быстро. Другая возможная причина – сдавление нерва в результате воспаления и отека сухожилий, которые также лежат в кистевом канале.
Частота заболевания
Синдром запястного канала может развиваться у любого человека и обычно является двусторонним. Доктора полагают, что до десяти процентов населения проявляют симптомы, но не все случаи нуждаются в лечении.
Каждый год трое из 1000 человек впервые диагностируют туннельный синдром запястья. Женщины в три раза чаще страдают, чем мужчины. Синдром запястного канала обычно возникает впервые в возрасте от 40 до 70 лет. У детей встречается редко.
Симптомы
Сдавливание нервного ствола развивается постепенно и в том же темпе нарастает интенсивность симптомов. В начальной стадии синдром практически не проявляется: у человека может возникать лишь чувство дискомфорта при продолжительной нагрузке на участок тела, в котором произошло ущемление нерва. По мере сужения канала происходят все более значимые нарушения функций нерва, которые проявляются следующими симптомами:
- болезненность в пораженной зоне, усиливающаяся после физических нагрузок;
- боль может возникать в состоянии покоя (чаще всего в ночное время);
- в периферийном участке тела (том, который находится дальше точки ущемления нерва) ощущается онемение, покалывание;
- при попытке «растянуть» пораженный сустав или связку или при простукивании этой зоны боль усиливается.
- При значительном сужении туннеля, к перечисленным симптомам присоединяются более выраженные:
- тугоподвижность пораженного сустава;
- ухудшение тонуса мышц в зоне сдавливания нерва;
- при одновременном напряжении симметричных мышц (например, при сжимании обеих ладоней в кулаки), мышцы на пораженной конечности менее выражены, что свидетельствует об их атрофии.
Одним из отличительных признаков туннельной невропатии является то, что при ущемлении нерва в крупном сочленении (лопатка, локоть, бедро), болезненность может проявляться на значительном расстоянии от пораженной зоны, что затрудняет диагностику. Так, например, при боли в плече, сопровождающейся онемением плеча, предплечья или верхней части спины, сдавливание нерва может быть как в локтевом суставе, так и в лопатке.
Симптоматическая картина
Патологический процесс характеризуется наличием болевого ощущения и покалывания на подошвенной поверхности на протяжении нескольких месяцев либо лет. На начальных этапах патологии больные предъявляют жалобы на болевой синдром на подошве во время ходьбы, а далее возникает спонтанным образом в ночное время. Болевой синдром распространяется от ступни и до ягодицы по задней плоскости нижней конечности, усиливается во время разгибания стопы. Спустя некоторое время (года) возникает слабость в фалангах ступни. На чувство жжения, онемения и покалывания в ступне жалуются примерно 60% больных. Симптоматика усиливается либо уменьшается на протяжении многих лет, происходит обострение в период ношения некомфортной обуви.
Объективный осмотр больного позволяет выявить болезненность во время пальпирования и перкутирования нерва у предплюсневого канала, иррадиирование болевого ощущения и онемения в ступню (95-95%), болезненность при пальпировании вдоль седалищного нерва от ступни и до ягодицы (1/2 случаев), гипестезию подошвенной плоскости (60%), гипотонию подошвенных супинаторов ступни и пальцев (70%), гипотрофические явления мышечных волокон стопы (65%); трудность или вообще неспособность хождения «на цыпочках» (95%). Наблюдаются парестезии в ступне (63%).
Симптомы Тинеля и Фалена наблюдаются в 2/3 случаев. Слабость подошвенных супинаторов ступни и пальцев
Осложнения
Чаще всего туннельная невропатия переходит в хроническое состояние, когда обострения заболевания чередуются с периодами ремиссии (бессимптомного течения болезни).
Хорошей новостью для людей, страдающих от туннельного синдрома, станет то, что патология крайне редко выходит за пределы пораженной зоны и самое худшее, что может случиться — усиление симптомов и болевого синдрома.
Таким образом, это состояние не представляет опасности для жизни. Но оно способно очень сильно нарушить ее качество. Боль, с течение времени становящаяся все продолжительней и сильнее, может вызвать нарушения сна, аппетита, стать причиной крайней раздражительности и в итоге привести к другим заболеваниям нервной системы, таким как хроническая бессонница, анорексия, булимия и пр.
Диагностика
при постоянных нагрузках на этот участок изменения закрепляются и становятся постоянными
В первую очередь врач, обследующий больного, исключает другие заболевания, имеющие симптомы, схожие с клинической картиной туннельной невропатии. Среди таких заболеваний артрит, артроз, невралгия, миалгия и пр.
После этого, для уточнения диагноза используются неврологические тесты, предназначенные для выявления повреждений в нервном стволе. Чаще всего применяется тест, называемый «симптомом Тинеля», при котором врач простукивает кожу над каналом, в который заключен поврежденный нерв. При туннельном синдроме больной чувствует онемение, покалывание, точечный зуд (так называемое «чувство ползающих мурашек»). Если синдром развился в зоне, недоступной для проведения теста Тинеля, может назначаться электромиография, исследующая способность нерва к проведению импульсов.
Обследования и диагностика
ЭНМГ обследование при туннельном синдроме запястья
В первую очередь доктор осматривает мышцы и артерии, проверяет, не произошла ли мышечная атрофия. В случае атрофированной мышцы большого пальца, пострадавший человек больше не может двигать большим пальцем. Как правило, тестом служит просьба врача взять в руку бутылку. В зависимости от стадии мышечной атрофии — это либо едва возможно, либо совсем не получается (положительный тест бутылки).
Чувствительность проверяется врачом похлопыванием по ладони пациента. Если пациент не воспринимает это прикосновение, чувствительность поверхности нарушена.
Чувство осязания и мелкая моторика пальцев проверяются возможностью пациента поднимать монеты или скрепки для бумаг. Если это не удается, то осязание нарушено.
Если врач еще не уверен в диагнозе он проводит провокационные тесты:
- Тест Хоффмана-Тинеля: поколачивание (перкуссия) по ходу срединного нерва вызывает боль и дискомфорт у пациента.
- Тест Фалена: для этого теста пациент должен сложить руки ладонями за спину, что сделает запястья более изогнутым. Если боль усиливается — это положительный признак Фалена, а также показатель синдрома запястного канала.
Неврологическое инструментальное тестирование
Абсолютно уверенным, что туннельный синдром присутствует, можно быть только после неврологического обследования. Электронейромиография (ЭНМГ) измеряет, как срединный нерв проводит полученные импульсы и передает на мышцы. Электроды во время обследования устанавливают на кожу, а скорость проводимости срединного нерва сравнивается с проводимостью другого здорового нерва. Обследование обычно безболезненно.
Рекомендуем
Рекомендуем прочесть статью о занятиях йогой при лечении суставов. Как йога помогает в процессе воостановления при артритах, какую программу для занятий желательно выбрать, как упражнения способствуют снятию боли вы сможете подробнее узнать из этой статьи.
Дополнительные исследования
Чтобы исключить другие заболевания с аналогичными симптомами (дифференциальный диагноз), врач часто исследует область локтя, шеи и плеча, где нерв также может быть сужен:
- Ультразвуковое исследование (сонография) мягких тканей кисти и предплечья определяет, насколько далеко проложен кистевой туннель.
- Рентгенологическое обследование используется для проверки того, ответственны ли за компрессию изменения в костях и суставах запястья.
- Магнитно-резонансная томография (МРТ) проводится, если врач подозревает, что причиной симптомов может быть опухоль.
Лечение
Лечение туннельной невропатии направлено на снятие воспалительного процесса и устранение отеков в пораженной зоне, избавление пациента от боли и предупреждение более сильного ущемления нерва.
Медикаментозное лечение
Среди медицинских препаратов свою эффективность подтвердили следующие группы:
- нестероидные противовоспалительные препараты (НПВП), такие как Ибупрофен, Кеторолак, Индометацин, Нимесулид и пр., помимо снятия воспаления обеспечивают обезболивающий эффект;
- гормональные препараты (Гидрокортизон, Преднизолон) вводятся в пораженную зону с помощью инъекции и/или наносятся на эту зону в виде мази;
- хлористый кальций вводится инъекционно, внутривенно, для снятия воспаления и стабилизации реакции иммунной системы;
- витаминные препараты назначаются для улучшения проводимости нервных сигналов и нормализации кровообращения в области сдавливания нерва.
Физиотерапия
При лечении туннельной невропатии рекомендуется курс тепловых физиотерапевтических процедур, с применением противовоспалительных и гормональных препаратов (электрофорез, фонофорез) и рефлексотерапия, нормализующая функции нервной системы.
Лечебная физкультура назначается в индивидуальном порядке, в зависимости от результатов обследования и степени сдавливания нерва — в ряде случаев при туннельной невропатии рекомендуется исключить любые нагрузки на пораженный сустав.
Хирургическое лечение
В тех случаях, когда консервативное лечение туннельного синдрома оказалось неэффективным, врач может рекомендовать оперативное лечение. Во время операции, которая проводится под общей анестезией и продолжается около часа, хирург иссекает утолщения в тканях, сдавливающих нерв, что позволяет восстановить его функции.
К недостаткам такого метода лечения относится то, что заранее невозможно спрогнозировать, насколько операция будет эффективной. В небольшом проценте случаев (порядка 2-3%) у больных после хирургического вмешательства наблюдается усиление симптомов.
Неврологические осложнения сахарного диабета: синдром запястного канала
Сахарный диабет (СД) занимает седьмое место в мире среди причин снижения качества жизни, в частности вследствие неврологических осложнений. При СД широко распространены туннельные (компрессионные) невропатии, главным образом – синдром запястного канала (СЗК). На сегодняшний день основой его патогенеза признана модель двойного повреждения. Исходя из клинических проявлений, выделяют три стадии СЗК. На ранних стадиях отмечаются характерные ночные боли и покалывания, локализующиеся преимущественно в дистальных отделах кисти и зоне иннервации срединного нерва. Позднее присоединяются скованность и неловкость в кисти в дневное время. При длительном течении – атрофия мышц тенара. Диагноз СЗК ставится на основании клинических проявлений. Однако могут использоваться тесты и электронейромиография. Последняя позволяет определить тип невропатии (аксональная или демиелинизирующая), тяжесть процесса и исключить другие причины повреждения нерва. Терапия СЗК при СД предполагает применение немедикаментозных, медикаментозных и хирургических методов в зависимости от стадии заболевания и выраженности симптомов. Наиболее простыми немедикаментозными способами лечения считаются иммобилизация кисти и изменение двигательного стереотипа. Фармакотерапия предусматривает назначение нестероидных противовоспалительных препаратов, антиконвульсантов и антидепрессантов, витаминов группы В и альфа-липоевой кислоты. В отсутствие эффекта показано оперативное вмешательство.
Патогенез СЗК при СД (модель двойного повреждения)
Клинические стадии СЗК
Введение
Сахарный диабет (СД) занимает седьмое место среди причин снижения качества жизни, в том числе вследствие неврологических осложнений [1]. К наиболее частым относится диабетическая невропатия (ДН). По некоторым данным, она встречается с частотой до 50% [2]. В масштабном исследовании EURODIAB диабетическая невропатия отмечалась у 28% больных СД [3]. Учитывая, что в мире насчитывается около 415 млн пациентов с СД, порядка 140 млн страдают ДН [4].
В 2011 г. Торонтская группа экспертов по диабетической невропатии представила обновленную классификацию, а также критерии диагностики и оценки тяжести заболевания [1, 5]. Согласно данной классификации выделяют генерализованные и фокальные/мультифокальные формы ДН. К первой относятся типичная дистальная сенсомоторная и атипичная сенсорная (острая, болевая) невропатии, ко второй – множественные мононевропатии, краниальные невропатии, туннельные невропатии и пояснично-грудная радикулопатия. При этом 80% случаев приходится на хроническую дистальную симметричную сенсорную и сенсомоторную полиневропатии [6].
Среди фокальных/мультифокальных невропатий чаще встречаются туннельные (компрессионные) невропатии, преимущественно синдром запястного канала (СЗК), или карпальный туннельный синдром.
Причиной СЗК являются сдавление и растяжение срединного нерва в остеофиброзном канале. Нерв располагается между поперечной связкой и костями запястья.
Заболевание может развиться на любой стадии СД и часто протекает бессимптомно.
Эпидемиология
Частота встречаемости СЗК в общей популяции составляет от 3 до 5%, риск развития в течение жизни может достигать 10% [7].
Среди пациентов с СД распространенность клинически выраженного СЗК, тем более асимптомного, выше. В Рочестерском исследовании таковой выявлен у 11 и 6% больных СД 1 и 2 типов соответственно [8]. В длительном наблюдательном Фремантльском исследовании с участием 1284 пациентов с СД частота встречаемости СЗК составила 5,5 случая на 1000 пациентов в год, что в 4,2 раза выше, чем в общей популяции [9]. По-видимому, существует и обратная зависимость, поскольку в ряде проспективных исследований у пациентов с СЗК зафиксировано повышение риска развития СД в два раза, у 80% больных – как минимум резистентность к инсулину [10, 11].
Распространенность СЗК среди больных СД варьируется от возраста, пола популяции, географии исследования, критериев диагностики и наличия у обследуемых факторов риска развития патологии.
B. Perkins и соавт. установили, что СЗК обусловлен симметричной дистальной сенсомоторной или сенсорной полиневропатией. Так, патология диагностирована у 14% пациентов с СД без полиневропатии и 30% больных СД с полиневропатией [12].
Более высокий риск развития СЗК в течение жизни зарегистрирован у лиц с СД 1 типа – после 54 лет болезни он увеличивается до 85% [13].
У пациентов с впервые выявленным СД патологию обнаруживали в 28% случаев, с длительным течением заболевания (в среднем 14,5 года) – в 63% [14, 15]. Эти данные позволили предположить, что риск развития СЗК в большей степени связан с продолжительностью СД, а не с возрастом пациентов.
Синдром запястного канала при СД, как и в общей популяции, чаще встречается у женщин. В исследовании с участием 146 пациентов с СД заболевание отмечалось в 39% случаев: у женщин – в 46%, у мужчин – в 28% [16].
Патогенез
В настоящее время в основе патогенеза СЗК при СД рассматривается модель двойного повреждения (рисунок) [17, 18]. Вследствие гипергликемии поражаются периферические нервы, которые становятся более восприимчивыми к вторичному повреждению местными компрессионными факторами, такими как давление, деформация и/или растяжение [19].
Поражение периферических нервов и замедление репаративных процессов в нервных волокнах при СД связывают не только с гипергликемией, но и недостатком инсулина, С-пептида. Указанные нарушения приводят к каскаду метаболических и сосудистых изменений.
Одним из основных механизмов повреждения нервной системы считается активация полиолового пути утилизации глюкозы. В результате в нервной ткани накапливаются сорбитол, фруктоза, активируется протеинкиназа С, истощается мио-инозитол и угнетаются Na+-К+-АТФазы. Как следствие, внутринейрональная аккумуляция Na+, задержка жидкости, отек миелиновой оболочки, уменьшение числа глиальных клеток аксонов и в конечном итоге дегенерация периферических нервов.
Значительная роль отводится окислительному стрессу, при котором образуются свободные радикалы, способствующие эндоневральной гипоксии.
Возможно участие таких факторов, как эндотелиальная дисфункция, поражение артерий мелкого калибра, генетическая предрасположенность [20].
Описанные выше эндоневральные, периневральные метаболические и сосудистые нарушения приводят к функциональным и структурным изменениям периферических нервов, что повышает вероятность компрессии в анатомически узких каналах. Доказано, что при сгибании/разгибании руки в запястье в восемь – десять раз повышается давление в кистевом туннеле и растягивается нерв, что обусловливает снижение внутриневральной микроциркуляции, повреждение миелиновой оболочки, нарушение функции аксонов, а также дисплазию соединительнотканных структур [18].
Клиническая картина
На ранних стадиях заболевания могут возникнуть боль и неприятные сенсорные симптомы – покалывание в кисти. Боль и онемение чаще локализуются в дистальных отделах кисти, зоне иннервации срединного нерва (области большого, указательного и среднего пальцев, а также на радиальной поверхности безымянного пальца). Указанные симптомы, как правило, появляются в ночное время.
В дневное время пациенты жалуются на неловкость в руке при выполнении движений, требующих ее сгибания в запястье [21]. Чтобы уменьшить онемение и неловкость, больным достаточно встряхнуть кистью (симптом встряхивания, или щелчка) [22].
При СЗК, как правило, поражается доминантная рука, однако возможно и двустороннее поражение [16].
В случае поражения вегетативных волокон, входящих в состав срединного нерва, отмечаются вегетативно-трофические нарушения: изменение температуры кисти, чувствительности к холоду и расстройство потоотделения [23].
В зависимости от наличия тех или иных симптомов выделяют три стадии СЗК (таблица) [21].
У большинства пациентов симптомы локализуются не только в зоне иннервации срединного, но и в зоне иннервации локтевого нерва, а также в области кисти, предплечья, локтя, плеча и шеи [24].
У некоторых пациентов наблюдается атипичное течение – например, писчий спазм либо слабость и боль в области плеча, или предплечья, или среднего пальца руки [21].
Однако СЗК при СД часто протекает бессимптомно и выявляется только при проведении электронейромиографии. Во время скрининга патологию обнаруживают у 30–36% лиц с впервые диагностированным СД. Этот факт подтверждает, что поражение проксимального сегмента нерва и/или сенсорных волокон при ДН может уменьшать вероятность развития клинически выраженного СЗК [25].
Болевой синдром
Болевой синдром при любой этиологии СЗК отмечается в 52–85% случаев [26, 27]. При этом болезненными могут быть и парестезии. Установлено, что парестезии и боль при СЗК встречаются с одинаковой частотой – 88,4 и 84,5% случаев соответственно [27].
При СЗК интенсивность боли не зависит от выраженности электрофизиологических изменений, пола, возраста и длительности заболевания. Она связана главным образом с неправильным представлением пациента о боли, депрессией, а также с наличием нескольких дополнительных источников боли [28]. При сочетании СЗК с болевой формой диабетической полиневропатии (ДПН) интенсивность боли может повышаться.
Несмотря на часто описываемые в литературе признаки невропатической боли (аллодиния, гиперпатия, прострелы по типу ударов электрическим током), данные о частоте ее встречаемости при СЗК противоречивы.
M. Sonohata и соавт. достоверный невропатический компонент боли с помощью опросника Pain DETECT обнаружили только у 10,5% пациентов с СЗК, вероятный – у 20,3%. При этом положительный результат тестирования был связан с пароксизмальным характером боли в ночное время [29].
В другом исследовании (все участники жаловались на ночные приступы боли) невропатический компонент наблюдался у 92% пациентов с болевым синдромом, что представляется более вероятным [30].
Однако боль при СЗК обусловлена не только невропатическим, но и ноцицептивным компонентом. При проведении биопсии у пациентов с симптоматическим СЗК выявлена повышенная экспрессия простагландина Е2 и сосудистого эндотелиального фактора роста, приводящая к сосудистой пролиферации и фиброзу с образованием рубцовой ткани вокруг срединного нерва и, как следствие, его сдавлению. Одновременно прогрессируют тендосиновит и воспаление синовиальной ткани сухожилий сгибателей. Это приводит к повышению давления в карпальном канале [31].
Диагностика
Диагностика СЗК основывается на клинических проявлениях.
В отсутствие выраженных сенсорных и моторных феноменов большое значение отводится сбору анамнеза. Следует установить время появления симптомов (ночные парестезии), провоцирующие факторы (положение руки, повторяющиеся движения), профессиональную вредность (использование в работе вибрационных инструментов), факторы, облегчающие симптомы (встряхивание кисти, изменение ее положения), наличие нисходящей или восходящей иррадиации боли [32].
Для верификации диагноза используются следующие инструменты [33]:
тест Тинеля. Постукивание неврологическим молоточком по запястью со стороны ладони в месте прохождения срединного нерва вызывает покалывание в пальцах. Чувствительность данного теста составляет от 26 до 79%, специфичность – от 40 до 100%;
тест Фалена. Сгибание/разгибание кисти на 90 градусов (при прямом локте) в течение 60 секунд или менее приводит к онемению и парестезиям в зоне иннервации срединного нерва. Тест позволяет подтвердить диагноз в 67–83% случаев, его специфичность варьируется от 47 до 100%;
тест Палея и МакМерфи. Считается положительным, если давление в точке проекции срединного нерва (1–2 см проксимальнее сгиба запястья) приводит к появлению или усилению боли и парестезий. Чувствительность теста составляет 89%, специфичность – 45%.
Проведенная перекрестная оценка чувствительности симптомов, а также тестов продемонстрировала наибольшую диагностическую значимость ночных акропарестезий (96%) и теста Палея и МакМерфи (89%).
Точность диагноза повышается (0,86), если по результатам трех тестов получен положительный ответ и отмечаются ночные акропарестезии.
Если результаты трех тестов отрицательные, акропарестезии отсутствуют, вероятность СЗК крайне низкая (0,0068) [33].
Для определения степени тяжести синдрома и обусловленных им функциональных нарушений разработан Бостонский опросник (Boston Carpal Tunnel Questionnaire – BCTQ) [34]. Результаты, полученные с помощью опросника, коррелируют не только в отношении клинической картины, но и в отношении электрофизиологических изменений. На сегодняшний день Бостонский опросник признан надежным и чувствительным инструментом стандартизации тяжести процесса и оценки результатов лечения.
В ряде публикаций продемонстрирована валидность данного способа диагностики у пациентов с СЗК на фоне СД и сопутствующей ДПН [35].
Дифференциальную диагностику СЗК проводят с артритом карпо-метакарпального сустава большого пальца, шейной радикулопатией (особенно корешков С6 и С7), плечевой плексопатией, ДПН, невропатией проксимальных отделов срединного нерва и др. [21].
Электрофизиологические методы исследования проводящей функции нерва являются базисом диагностики компрессионных невропатий, в частности СЗК [36]. Оценка проводящей функции двигательных и чувствительных волокон срединного нерва позволяет подтвердить компрессионную невропатию, признаком которой служат локальные изменения проводимости пораженного нерва в анатомически узких каналах.
Считается, что для диагностики СЗК более значимы параметры сенсорного ответа. Сенсорные волокна срединного нерва имеют большую долю толстых миелинизированных волокон с высокой потребностью в энергии, что обусловливает их большую восприимчивость к ишемическому и метаболическому повреждению. Электронейромиография также помогает определить тип невропатии (аксональная или демиелинизирующая), тяжесть процесса и исключить другие патологии.
Особенности проведения электродиагностики СЗК описаны в монографии Американской ассоциации нервно-мышечной и электродиагностической медицины (American Association of Neuromuscular & Electrodiagnostic Medicine – AANEM) [36, 37].
Так, у пациентов с СД и СЗК в отличие от общей популяции больных СЗК во избежание ложноположительного результата не рекомендуется сравнивать значения амплитуд и латентностей ответов срединного нерва со среднепопуляционными нормами, поскольку ряд факторов (возраст, пол, диаметр большого пальца, системные заболевания, ожирение и др.) могут повлиять на точность исследования. Более корректно сравнивать показатели, полученные у одного и того же больного на разных участках срединного нерва, например в области запястного канала и на интактном участке срединного нерва.
У пациентов с СД при подозрении на СЗК и ДПН в обязательном порядке проводятся сравнительные исследования срединного, локтевого и лучевого нервов [36, 37].
В последнее время широко используются ультразвуковые методы исследования периферических нервов. Они обладают рядом преимуществ: неинвазивность, отсутствие противопоказаний, сокращение времени проведения и др. [38]. Основными признаками туннельной невропатии при ультразвуковом исследовании считаются локальное утолщение нерва и увеличение площади поперечного сечения в проксимальном направлении от места локализации сдавления. Диагностическая ценность и специфичность ультразвукового исследования превышают 85% [39]. Менее распространенными признаками заболевания являются гипоэхогенная структура, уплощение нерва в месте компрессии, увеличение числа одиночных или множественных фасцикул, а также повышение васкуляризации нерва [39].
Магнитно-резонансная томография позволяет исключить редкие причины СЗК, такие как гемангиома, остеомиелит и деформация костей, артропатия Шарко.
Недавно был внедрен метод магнитно-резонансной трактографии, позволяющий оценить тяжесть морфологических изменений и воспаления. Однако его доступность пока ограничена [40].
Лечение и профилактика
Лечение СЗК предполагает применение немедикаментозных, медикаментозных и хирургических методов в зависимости от стадии заболевания и выраженности симптомов. К сожалению, приходится констатировать, что за помощью пациенты обращаются уже при развернутой стадии заболевания, чаще всего с жалобой на болевой синдром или атрофию мышц тенара.
Среди немедикаментозных методов на первом месте стоит изменение двигательных стереотипов (избегание движений в кисти и подъема тяжестей). В помощь пациентам проводятся образовательные программы. Показана также иммобилизация области повреждения, что позволяет прекратить или ограничить физическое воздействие и уменьшить отек. Добиться иммобилизации в зоне повреждения помогают шины, ортезы, брейсы, лонгета для запястного сустава. Однако, несмотря на наличие рандомизированных контролируемых исследований (РКИ) с шинированием до восьми недель, уровень доказательности данного метода признан умеренным.
Обсуждаются также возможности лазеротерапии, чрескожной электронейростимуляции, фонофореза глюкокортикостероидами, акупунктуры, лечебной гимнастики [27].
Медикаментозная терапия предполагает воздействие на различные компоненты болевого синдрома: ноцицептивный, невропатический и в ряде случаев дисфункциональный. Для воздействия на ноцицептивный компонент боли, а также для уменьшения воспаления показаны нестероидные противовоспалительные препараты (НПВП). Однако данная, широко исследованная при других нозологиях группа лекарственных средств при СЗК недостаточно изучена с позиций доказательной медицины [27].
В этой связи представляет интерес исследование эффективности препарата мелоксикам. У пациентов с СЗК препарат применяли в течение десяти дней. На фоне проводимой терапии снизилась интенсивность боли, а также уровень субстанции Р – одного из основных медиаторов боли. При этом снижение отмечено в синовиальной оболочке сухожилий (параневрально), но не в адвентициальной оболочке срединного нерва, что подтверждает избирательность действия препарата в отношении ноцицептивного компонента боли [41].
На сегодняшний день зарегистрирован ряд биоэквивалентных аналогов мелоксикама, в том числе российский препарат Артрозан, который производится в инъекционной и таблетированной формах.
При выборе НПВП необходимо учитывать риск развития желудочно-кишечных и сердечно-сосудистых осложнений и принять меры для снижения таковых [42].
В случае выявления невропатического компонента боли также целесообразно назначение антиконвульсантов (габапентина (Конвалиса), прегабалина), антидепрессантов (венлафаксина, дулоксетина, амитриптилина) [43].
Применение данных средств будет оправданно для облегчения боли как при ДПН, так и при СЗК. Однако если при болевой форме ДПН применение указанных препаратов имеет высокий уровень доказательности, то при СЗК исследован только габапентин. Габапентин продемонстрировал эффективность в отношении купирования боли при СЗК как в низкой (300–600 мг/сут), так и в средней терапевтической (1800 мг/сут) дозе. Длительность наблюдения составила от двух до шести месяцев [44–47].
При назначении габапентина следует соблюдать схему титрации дозы и учитывать возможность развития преходящих побочных эффектов, таких как головокружение и сонливость.
В России помимо оригинального габапентина зарегистрированы его аналоги, например препарат Конвалис. В российском исследовании последний подтвердил свою эффективность у больных ДПН [48].
В качестве дополнительных методов лечения СЗК, развившегося на фоне ДПН, следует рассматривать препараты альфа-липоевой кислоты (Октолипен) и витаминов группы В (Комбилипен).
При ДПН назначение альфа-липоевой кислоты признано патогенетически обоснованным из-за способности препарата связывать свободные радикалы и таким образом предупреждать нейрососудистые нарушения [49].
Результаты метаанализа РКИ по применению альфа-липоевой кислоты 300–600 мг внутривенно в течение двух – четырех недель у пациентов с ДПН свидетельствуют, что такая терапия способствует не только уменьшению боли, но и повышению скорости проведения возбуждения по нервам [50].
Учитывая особенности патогенеза СЗК на фоне СД и описанные выше функциональные и структурные изменения нервов, использование альфа-липоевой кислоты (Октолипена) у таких больных оправданно.
Кроме того, в одном из РКИ продемонстрирована большая эффективность комбинации габапентина и альфа-липоевой кислоты по сравнению с плацебо и монотерапией указанными препаратами в отношении облегчения невропатической боли [51].
В другом РКИ у пациентов с болевой формой ДПН сравнивали эффекты комбинации «габапентин + витамины группы В» и прегабалина. Через 12 недель лечения уменьшение боли на 30% удалось достичь на 900 мг габапентина плюс 100 мг витамина В1/20 мг витамина В12 и 300 мг прегабалина. Был сделан вывод, что комбинация габапентина с витаминами группы В позволяет снизить дозы габапентина, что в свою очередь улучшает переносимость и приверженность терапии [52].
При воздействии на ноцицептивный компонент боли важно учитывать синергизм витаминов группы В и НПВП. Установлено, что в одних случаях данная комбинация позволяет добиться лучшего анальгетического эффекта, чем монотерапия НПВП, в других – эффективность комбинации и монотерапии сопоставима, однако при использовании комбинации требуется меньшая доза НПВП, что повышает безопасность лечения [53, 54].
Среди инвазивных методов лечения СЗК наиболее исследованным являются инъекции глюкокортикостероидов в область туннеля запястья. В отношении купирования боли и уменьшения симптомов их эффект превышает плацебо, местные анестетики и НПВП.
Использование ладонного доступа более эффективно, чем введение иглы в область запястья, а проведение процедуры под контролем ультразвукового исследования обеспечивает ее точность.
В одном РКИ показана эффективность локальных инъекций лидокаина [27].
В отсутствие значимого эффекта от консервативного лечения показано оперативное. Хирургическое лечение СЗК заключается в декомпрессии срединного нерва путем рассечения поперечной связки запястья. Операция может быть открытого доступа (как обширного, так и минимального) либо эндоскопическая. Эти два подхода значимо не различаются в отношении уменьшения выраженности клинических проявлений и улучшения функционального состояния кисти. Однако в недавнем исследовании продемонстрировано преимущество второго [55].
Данные об эффективности хирургической декомпрессии при СЗК вследствие СД и идиопатическом СЗК противоречивы. В ряде длительных проспективных наблюдений отмечено, что отдаленный эффект хирургического вмешательства у пациентов с СЗК и СД несколько ниже, чем в общей популяции [56]. В других исследованиях различий между группами по отдаленным результатам лечения не выявлено [57].
Профилактика СЗК при СД заключается прежде всего в контроле массы тела и гликемии. Пациенту также необходимо правильно организовать рабочее место, если его профессиональная деятельность предполагает повышенную нагрузку на запястье (работа за компьютером, повторяющиеся движения и т.д.) [21, 27].
Заключение
СЗК, развившийся вследствие СД, особенно при длительном течении и наличии ДПН, встречается достаточно часто. Поэтому от врача требуется настороженность в отношении этой патологии и назначение дополнительных диагностических тестов для ее выявления на ранней стадии. Это позволит ограничиться консервативными методами лечения.
Коррекция образа жизни
Многие люди предпочитают «удобный» вариант лечения, при котором врач прописывает эффективные лекарства или процедуры, и от самого больного не требуется никаких действий. К сожалению, туннельная невропатия предполагает активное участие больного в процессе лечения.
Главным условием выздоровления или достижения продолжительной ремиссии является устранение стереотипных движений, которые привели к сдавливанию нерва. Нередко это становится единственным действенным мероприятием, облегчающим симптомы при туннельном синдроме.
Постарайтесь выполнять привычные действия здоровой рукой при локтевом, запястном или плечевом ущемлении нерва. Если это невозможно, сведите к минимуму нагрузку на больную руку: выполняйте ею только самые необходимые действия, перекладывая основную часть работы на здоровую.
Приобретите привычку спать на боку, противоположном больной руке, ноге или лопатке. Это позволит пораженной зоне «отдыхать» в течение вашего ночного сна и компенсировать таким образом дневные нагрузки.