Причины
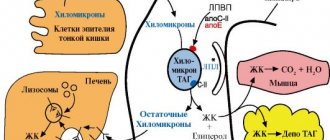
Синдром Помпе обусловлен мутацией в гене GAA, который расположен в хромосоме 17. Данный ген отвечает за кодирование лизосомного фермента кислой альфа-глюкозидазы. Она является важным катализатором процесса расщепления молекулы гликогена до глюкозы, которая участвует в энергетическом обмене клеток. Другими словами, происходит нарушение гликогенного обмена, что является причиной нехватки энергии для мышечных и нервных волокон, печени, миокарда.
Дистрофия, повреждение клеток происходит и по причине накопления гликозида в лизосомах. Наследование гена GAA происходит по аутосомно-рецессивному типу, т.е. больной получает мутантную аллель от обоих родителей. Форма заболевания влияет на выбор лечения, дальнейший прогноз.
Классификация
Болезнь Помпе у взрослых встречается редко. В основном гликогенозу подвержены дети. Сроки развития болезни, ее симптоматика определяют формы заболевания:
- Ранняя – проявляется при рождении либо на первых месяцах жизни, считается самой опасной формой болезни (смертность 100% в возрасте до 1 года).
- Поздняя – симптоматика наблюдается в 1-3 года. Частичное исчезновение альфа-глюкозидазы или снижение ее активности определяет позднюю форму синдрома Помпе.
- Ювенильная – развитие характерных признаков в 6-10 лет.
- Взрослая – развитие симптоматики происходит в диапазоне 20-40 лет. У больных наблюдается медленно прогрессирующие нарушения миокарда.
Болезнь Помпе: вместе мы сильные
15 апреля во всем мире пациентские организации и пациенты с болезнью Помпе проводят образовательные и информационные кампании для повышения осведомлённости широкой общественности об этом редком наследственном заболевании с аутосомно-рецессивным механизмом наследования.
Ребенок с болезнью Помпе
Точная распространенность болезни Помпе неизвестна. По данным разных авторов, частота болезни, в зависимости от страны и этнической принадлежности, варьирует в диапазоне от 1:40.000 до 1:300.000.[1]При данном диагнозе в результате нехватки определенного фермента в клетках мышц и сердца больного накапливается особое вещество гликоген[2].
В семьях, где родители являются носителями болезни Помпе, риск рождения больного ребенка составляет 25% на каждую беременность.[3] В случае, если одному ребенку поставили этот диагноз, это не значит, что все дети будут больны, но нужно обязательно обследовать всех братьев и сестер.
Характерный признак заболевания – прогрессирующая мышечная слабость, в том числе скелетной и дыхательной мускулатуры[4]. Поражение сердечной мышцы проявляется в основном в начале заболевания в очень раннем возрасте. Такая форма заболевания называется младенческой. Она быстро прогрессирует и приводит к гибели на первом году жизни.5 В случаях юношеской или взрослой форм прогрессирование болезни включает в себя нарастающую слабость мышц туловища и ног, нарушение походки, одышку, дыхательную недостаточность, затруднение при жевании и глотании, вследствие быстрой утомляемости жевательных мышц. Без терапии, с течением времени, симптомы болезни нарастают. Многие пациенты перестают самостоятельно ходить и постепенно становятся зависимыми от аппарата искусственной вентиляции легких, поскольку происходит поражение мышц, ответственных за дыхание. [5], [6]
В отличии от многих других редких заболеваний, для пациентов с болезнью Помпе существует ферментозаместительная терапия, эффект от которой во многом зависит от того, когда пациент начал получать лечение. При своевременном и регулярном получении недостающего фермента, можно остановить или замедлить прогрессирование заболевания, что позволяет людям с этой болезнью вести активную социальную жизнь.
Ключевую роль в лечении болезни Помпе занимает ранняя диагностика.
«При диагностике редких заболеваний в целом и болезни Помпе в частности большая ответственность лежит на врачах первичного звена. Очень важно чтобы врач вовремя заподозрил «редкий диагноз» и направил пациента на обследование в случае необходимости. Но и сам пациент тоже должен быть довольно настойчивым и в тоже время иметь терпение, чтобы найти причину болезни и возможно провести обследование всей семьи. Нужно понимать, что нет «орфанного» врача, есть врач, который хочет разобраться. В среднем около 7 врачей должен обойти пациент с редким заболеванием, прежде чем ему поставят диагноз. И это не только в России, это во всем мире!», — подчеркнула Е. Ю. Захарова, заведующая лабораторией наследственных болезней обмена веществ Медико-генетического научного центра РАН, доктором медицинских наук.
«Первые изменения в организме дочери мы заметили во время диспансеризации по ДМС. Процесс постановки диагноза был долгим, — отмечает Е., мама пациентки с болезнью Помпе, — Сначала ставили недифференцированный гепатит, но лечение не помогало. Потом нашли доктора, которая и помогла поставить диагноз – болезнь Помпе. В общей сложности мы пытались установить диагноз полтора года. После начался долгий период принятия диагноза, изучения информации и адаптации к жизни с болезнью.»
В России заболевание считается редким (орфанным), если его распространенность встречается не более 10 случаев на 100 000 населения.[7] Чаще всего они являются генетическими и проявляются в детстве7, но также дебют заболевания может произойти во взрослом возрасте. При адекватном лечении и систематическом применении лекарственных препаратов люди с орфанными заболеваниями могут вести активную жизнь и быть полноценными членами общества.[8]
[1] https://www.pediatr-russia.ru/sites/default/files/file/kr_pompe.pdf
[2] Hirschhorn, Rochelle and Arnold J. J. Reuser. Glycogen Storage Disease Type II: Acid Alphaglucosidase (Acid Maltase) Deficiency. In: Scriver C, Beaudet A, Sly W, Valle D, editors. The Metabolic and Molecular Bases of Inherited Disease. 8th Edition. New York: McGraw-Hill, 2001. 3389-3420.
[3] https://pompe.rare-diseases.ru/
[4] Kishnani PS, Steiner RD, Bali D, et al. Pompe disease diagnosis and management guideline. Genet Med 2006; 8:267-88
[5] Van den Hout HM, Hop W, van Diggelen OP, et al. The natural course of infantile Pompe’s disease: 20 original cases compared with 133 cases from the literature. Pediatrics 2003; 112:332-40.
[6] Van der Beek Naet al. Clinical features and predictors for disease natural progression in adults with Pompe disease: a nationwide prospective observational study. Orphanet J Rare Dis. 2012 Nov 12;7:88
[7] https://spiporz.ru/redkie-zabolevaniya/
[8] https://philanthropy.ru/intervyu/2016/03/11/35529/
Симптомы
Характерные признаки генетической болезни зависят от формы гликогеноза. Симптоматика такова:
| Ранняя | Поздняя и Ювенильная | Взрослая |
| Расстройство дыхания | Мышечная атрофия (вплоть до диафрагмы) | Нарастающая мышечная слабость |
| Вздутие живота | Проблемы с координацией движений | Утренняя головная боль |
| Гипертрофия мышц при пальпации | Позднее начало ходьбы | Сонливость или бессонница |
| Кардиомиопатия | Дисфагия (нарушения глотания) | Сколиоз грудного отдела |
| Изменение размеров языка (увеличение) | Нарушение дыхательных функций | Одышка при физической нагрузке |
| Расстройство глотания, вялое сосание | Частые простуды, ОРВИ | Ортопноэ (нарушение дыхания в горизонтальном положении) |
| Увеличение печени, сердца | Гепатоспленомегалия (увеличение селезенки, печени) | Признаки сердечной недостаточности |
| Аритмия (нарушение сердечного ритма) | Задержка роста |
Статьи по теме
- Растворы для ингаляции небулайзером при бронхите для детей и взрослых с описанием
- Заболевания нижних конечностей — признаки, классификация, диагностика, терапия и профилактика
- Миопатия – что это такое у детей и взрослых
Проявления поздней инфантильной и ювенильной формы
При поздней и ювенильной форме патологии клиническая картина очень схожа. Отличие заключается лишь в сроках появления первых признаков, а именно выявления мышечной слабости. Позже симптоматика дополняется нарушениями работы сердечной мышцы. Через несколько месяцев после появления первых признаков врачи диагностируют формирование мышечной дистрофии скелетной мускулатуры и кардиомегалии.
Длительность течения заболевания в каждом конкретном случае может быть разной, но средний срок составляет 9-12 лет. При этом могут проявиться и косвенные симптомы патологии в виде головных болей, ночных апноэ, частых респираторных заболеваний различной сложности. Отсутствие терапии приводит к летальному исходу вследствие сердечной недостаточности.
Диагностика
Для выявления синдрома Помпе используют несколько методов диагностики. Начальный этап постановки диагноза требует выполнения общих процедур:
- анализ семейного анамнеза;
- определение основных симптомов с помощью осмотра, пальпации, сбора данных;
- лабораторные анализы (общий и биохимический анализ крови, генетические тесты, пробы методом ПЦР);
- МРТ, КТ, ЭКГ, ЭхоКГ;
- рентгенография грудной клетки;
- ультрасонография брюшной полости – получение изображения органов и тканей.
Уточнение диагноза требует применения специфической диагностики. К ее методам относятся:
- Амниоцентез – исследование околоплодной жидкости на предмет генетических отклонений, проводится в перинатальный период.
- Установление степени активности кислой альфа-глюкозидазы – проводится методом проверки лейкоцитов, а также сухих пятен крови.
- ДНК-исследования – изучение GAA гена на предмет мутации.
- Биопсия пораженной мышечной ткани – наличие скопления гликогена, полостей в цитоплазме.
Поздняя форма синдрома Помпе диагностируется с помощью определенных способов. К ним относятся:
- Полисомнография – исследование показателей крови во время сна, для установления апноэ.
- Электромиография мышц скелета – оценка электрической активности мышечной массы.
- Установление жизненной емкости легких – определение поражения диафрагмы с помощью разницы показателей стоя и лежа.
Диагностика[править | править код]
Диагноз данной редкой наследственной патологии верифицируется на основании лабораторного исследования степени активности фермента — кислой α-1,4-глюкозидазы (мальтазы) в крови (метод «сухого пятна»)[7] или тканях организма (кожных фибробластах, мышечной ткани, лейкоцитах).
Заболевание в встречается в различных клинических формах:
- классическая (инфантильная) форма болезни Помпе и
- болезнь Помпе с поздним началом (в детском, подростковом возрасте и у взрослых).
Этапы диагностического поиска[править | править код]
Классическая (инфантильная) форма:
- этап: выявление группы риска.
- основные клинические проявления: выраженная мышечная гипотония (синдром «вялого ребёнка»);
- задержка моторного развития;
- частые инфекционные заболевания верхних дыхательных путей (ОРЗ);
- наличие признаков дыхательной недостаточности;
- расстройства дыхания во сне;
- кардиомегалия в сочетании с кардиомиопатией;
- сердечная недостаточность;
- макроглоссия;
- гепатомегалия;
- спленомегалия;
- гипотрофия
- лабораторная диагностика: повышение уровня креатинфосфокиназы, лактатдегидрогеназы, АлАТ, АсАТ в сыворотке крови.
- инструментальные методы диагностики:
- поиск наличия признаков поражения миокарда и/или сердечного ритма;
- ЭКГ;
- ЭхоКГ;
- МРТ;
- рентгенография органов грудной полости
- этап: специфическая диагностика.
- диагностика: для всех пациентов группы риска болезни Помпе — биохимический анализ активности кислой мальтазы в крови методом сухих пятен
- верификация: повторное измерение уровня активности кислой мальтазы в крови альтернативным методом (например, определение активности этого фермента в лейкоцитах периферической крови)
- этап: дополнительные методы диагностики.
- при наличии типичной клинической картины на фоне «нормальной» активности кислой мальтазы в крови показано проведение ДНК-диагностики дефектного гена (GAA).
- морфологический анализ мышечной ткани (биопсия) позволяет выявить специфические изменения, однако их отсутствие не исключает наличия болезни Помпе.
Диагностический алгоритм болезни Помпе с поздним началом:
- этап: выявление группы риска.
- основные клинические проявления: прогрессирующая мышечная слабость тазового и плечевого пояса (на начальных стадиях болезни преобладает слабость в ногах);
- затруднение при ходьбе, подъёме по лестнице, вставании из положения сидя;
- боли в мышцах;
- дыхательная недостаточность;
- ортопноэ;
- частые инфекционные заболевания дыхательных путей;
- дневная сонливость;
- головная боль по утрам;
- ночная гиповентиляция лёгких;
- снижение массы тела у детей и подростков;
- гипотрофия
- лабораторная диагностика: повышение уровня креатинфосфокиназы, лактатдегидрогеназы, АлАТ, АсАТ в сыворотке крови.
- инструментальные методы диагностики:
- выявление миопатического паттерна в ходе проведения миографии скелетных мышц конечностей;
- выявление расстройств дыхания во время сна (эпизоды апноэ и снижение степени оксигенации крови) в ходе проведения полисомнографии;
- выявление значительной разницы результатов измерения форсированной жизненной ёмкости лёгких (ФЖЕЛ) в положении лежа и сидя более, чем на 10 % от исходной величины ФЖЕЛ — ранний признак специфического поражения диафрагмы при болезни Помпе.
- этап: специфическая диагностика.
- диагностика: для всех пациентов группы риска болезни Помпе — биохимический анализ активности кислой мальтазы в крови методом сухих пятен
- верификация: повторное измерение уровня активности кислой мальтазы в крови альтернативным методом (например, определение активности этого фермента в лейкоцитах периферической крови)
- этап: дополнительные методы диагностики.
- при наличии типичной клинической картины на фоне «нормальной» активности кислой мальтазы в крови показано проведение ДНК-диагностики дефектного гена (GAA).
- морфологический анализ мышечной ткани (биопсия) позволяет выявить специфические изменения, однако их отсутствие не исключает наличия болезни Помпе.
Лечение
Синдром Помпе полному излечению не поддается. Специфической терапией считается пожизненное применение ферментозаместительного лечения. Оно осуществляется с использованием рекомбинантной кислой альфа-глюкозидазы. Вещество помогает улучшить качество жизни пациента, замедлить прогрессирование симптомов, снизить риск появления осложнений.
В России единственно доступным препаратом данной группы является Майозайм. Его применяют капельно внутривенно для восстановления пораженных органов и систем. Использование рекомбинантного фермента снижает смертность на 99%, а риск осложнений дыхания – на 92%. Препарат назначается для постоянного приема.