Классификация
Высокая концентрация белка может наблюдаться и у абсолютно здоровых людей (физиологическая гиперпротеинемия). Такое происходит при беременности, взятие крови на анализ через 30 минут после длительного пребывания в горизонтальном положении. По этиопатогенезу различают 2 типа гиперпротеинемий:
- Гемоконцентрационные (ложные). Данный вид развивается в результате сгущения крови вследствие уменьшения жидкой ее части. Встречается при диарее, обширных ожогах, обильном потоотделении.
- Гиперсинтетические (истинные). Возрастание уровня протеина происходит из-за усиления его продукции. Характерно для инфекционных и неинфекционных, острых и хронических воспалительных заболеваний, болезней накопления, моноклональных гаммапатий.
Гиперпротеинемия может возникать за счет увеличения какой-либо белковой фракции. Выделяют:
- Гиперальбуминемию. Увеличение фракции альбуминов. Встречается в основном при дегидратации организма.
- Гиперглобулинемию. Повышение содержания в крови альфа-бета-гаммаглобулинов, иммуноглобулинов. Наблюдается при инфекциях, различных аутоиммунных, хронических воспалительных заболеваниях.
- Парапротеинемию. Характеризуется продукцией структурно аномальных белков – макроглобулинов, белка Бенс-Джонса. Данные белки появляются при макроглобулинемии Вальденстрема, множественной миеломе.
Причины ложной гиперпротеинемии
Развитие данной разновидности гиперпротеинемии связано с увеличением относительного содержания белка из-за значительного уменьшения количества жидкости в крови. При этом гиперпродукция белка отсутствует. Типично для:
- острых кишечных инфекций (сальмонеллеза, дизентерии), сопровождающихся неукротимой рвотой и профузной диареей;
- обширных ожогов;
- длительной гектической лихорадки с обильным потоотделением.
Степень гиперпротеинемии почти всегда умеренная и быстро регрессирует после коррекции водного дефицита.
Гиперпротеинемия
Причины истинной гиперпротеинемии
Инфекции
Одна из наиболее распространенных причин данного состояния. При попадании инфекционного агента (бактерий, вирусов, паразитов) в организм человека происходит их фагоцитирование. В процессе фагоцитоза микроорганизмов лейкоциты начинают вырабатывать пептидные факторы и провоспалительные цитокины (интерлейкины, интерферон, фактор некроза опухолей).
Эти вещества в совокупности с активацией симпато-адреналовой системы стимулируют образование в печени белков острой фазы (С-реактивного белка, белков системы комплемента, серомукоидов) и иммуноглобулинов (антител) в B-лимфоцитах. Возрастание концентрации белка отмечается примерно через 5-6 часов после начала острого или обострения хронического инфекционного заболевания и достигает максимума через 48-72 часа.
Уровень гиперпротеинемии коррелирует с активностью патологического процесса, однако редко достигает больших значений (степень в основном умеренная). Показатели белка выше при бактериальных (пневмония, пиелонефрит) и паразитарных (малярия, трипаносомоз) инфекциях, а также при генерализованных инфекциях любой этиологии (сепсис). Концентрация протеина достаточно быстро нормализуется после стихания воспаления под влиянием специфической терапии.
Воспалительные заболевания
К данной группе преимущественно относятся патологии аутоиммунной природы – ревматоидный артрит, системные болезни соединительной ткани (СКВ, системная склеродермия), воспалительные заболевания кишечника (болезнь Крона, неспецифический язвенный колит). Точный патогенетический механизм гиперпротеинемии при хронических воспалительных аутоиммунных заболеваниях до сих пор неизвестен.
Предполагается, что под влиянием неизвестного этиологического фактора происходит усиленная выработка воспалительных белков (главным образом СРБ) и глобулинов (аутоантител) в рамках иммунной аутоагрессии. Гиперпротеинемия появляется только в период обострения заболевания, почти всегда незначительная или умеренная. После наступления рецидива гиперпротеинемия может сохраняться некоторое время (от нескольких дней до нескольких недель).
Моноклональные гаммапатии (парапротеинемии)
Эту группу заболеваний стоит подозревать при высокой и длительно сохраняющейся гиперпротеинемии. К ним относятся множественная миелома (миеломная болезнь Рустицкого-Каллера), макроглобулинемия Вальденстрема, болезнь легких цепей. В основе патогенеза лежит гиперпродукция опухолевыми плазматическими клетками белков-парапротеинов, аномальных по молекулярному строению и иммунологическим свойствам: макроглобулинов, моноклональных иммуноглобулинов, легких цепей каппа или лямбда.
Отличительной чертой данного вида гиперпротеинемии является то, что она служит не только диагностическим маркером, но и напрямую определяет степень тяжести болезни. Из-за особенностей физических свойств парапротеинов они в несколько раз повышают вязкость крови, что значительно нарушает кровообращение во всех органах и тканях, особенно в головном мозге.
Гиперпротеинемия при этих заболеваниях может привести к коматозному состоянию (парапротеинемическая кома). Концентрация белка нарастает медленно, в течение нескольких лет, параллельно опухолевой прогрессии. Уровень общего белка увеличивается примерно на 15-20%. Его снижение происходит только после удаления избытка паарпротеинов из системного кровотока с помощью экстракорпоральных методов очищения крови (плазмаферез).
Редкие причины
- Различные формы амилоидоза.
- Семейная средиземноморская лихорадка (периодическая болезнь).
- Криоглобулинемия.
Диагностика
Сама по себе гиперпротеинемия представляет собой довольно редкое явление, поэтому ее обнаружение требует особого внимания и дифференциальной диагностики. При получении биохимического анализа крови с высоким содержанием белка сначала необходимо обратиться к врачу-терапевту. Важное значение имеют анамнестические данные: возраст пациента, диагностированные ранее хронические заболевания.
Уточняется, что предшествовало появлению высокого уровня протеина – обильное потоотделение, длительная диарея и т.д. Также при физикальном осмотре больного выясняется наличие тех или иных симптомов, что может помочь в установлении причины отклонения в анализах, например, лихорадка при инфекциях, боли в суставах при аутоиммунной ревматологической патологии, боли в костях и повторяющиеся носовые кровотечения при парапротеинемиях. Для выявления причины данного лабораторного феномена назначается следующее обследование:
- Анализы крови. В общем анализе крови отмечаются маркеры воспаления – увеличение СРБ и скорости оседания эритроцитов. Данные показатели особенно высоки при выраженном обострении ревматических заболеваний и парапротеинемиях. Могут выявляться лейкоцитоз, анемия. При гиперпротеинемии обязательно определяется содержание отдельных фракций – альбуминов, альфа- и гамма-глобулинов.
- Анализы мочи. Общий анализ мочи нередко показывает протеинурию. При множественной миеломе в моче обнаруживается белок Бенс-Джонса.
- Электрофорез белков. Данное исследование проводится для получения более точной и полной информации о содержании различных белковых фракций. Для моноклональных гаммапатий характерна высокая концентрация М-протеина.
- Идентификация инфекционного возбудителя. Для выявления инфекционного агента выполняются микробиологические, вирусологические исследования: бактериальный посев мокроты, мочи, крови на питательные среды; методами ИФА и ПЦР проверяется наличие ДНК микроорганизмов или антител к ним.
- Обследование на аутоиммунную патологию. Определятся титр аутоантител – ревмофактора, антител к циклическому цитруллинированному пептиду, к ДНК и пр. При подозрении на воспалительные болезни кишечника информативен анализ на фекальный кальпротектин.
- Рентген. При аутоиммунных артропатиях на рентгенограмме визуализируется сужение суставной щели, околосуставной остеопороз. Для миеломной болезни характерны множественные очаги остеолизиса и остеодеструкции, которые особенно отчетливо видны в области черепа («симптом пробойника»)
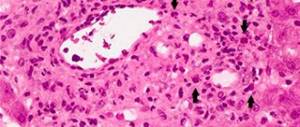
- Гистологические исследования. Получение аспирата костного мозга путем трепанобиопсии или стернальной пункции назначается только в том случае, если подозревается злокачественная природа гиперпротеинемии. Могут быть обнаружены следующие изменения – это лимфо- или плазмоклеточная инфильтрация, фиброз стромы.
Гиперпротеинемия диагностируется по результатам биохимического анализа крови
Методы диагностики отечного синдрома
Для начала лечения этого патологического состояния сначала очень важно определить первопричину его появления. Больной идет на прием к терапевту, но в дальнейшем может потребоваться консультация узких специалистов. В первую очередь врач проводит осмотр пораженной области. Для выявления причины возникшей проблемы может быть показано проведение таких исследований, как:
- электрофорез белков;
- определение содержания Т3 и Т4;
- радиоиммунологическое исследование;
- функциональные печеночные пробы;
- эхокардиография;
- радиоизотопная ангиография сердца;
- компьютерная томография;
- радиография;
- флебография;
- доплеровское ультразвуковое исследование вен;
- лимфангиография.
Консультация эндокринолога и кардиолога особенно важна пациентам, у которых развился хронический отек. Только после выявления первопричины патологии и оценки общего состояния больного принимается решение о необходимости госпитализации и выборе лечения.
Симптомы
Симптомы гипопротеинемии определяются процессами, которые запускаются в организме при дефиците белка в крови:
- снижается коллоидно-астматическое давление крови, в результате чего жидкость из сосудистого русла переходит в окружающие ткани;
- замедляется перенос питательных веществ к клеткам внутренних органов;
- уменьшается синтез антител.
Вследствие данных изменений возникают следующие патологические проявления:
- Образуются диффузные (по всему телу) или ограниченные отеки. Во втором случае чаще всего отекают ноги.
- Снижается сопротивляемость организма инфекциями. Угнетение иммунитета особенно выражено, если наблюдается гипопротеинемия у детей.
В тяжелых случаях может произойти выпот жидкости в различные органы и ткани:
- в околосердечную сумку (перикард) – развиваются аритмия и перикардит;
- в плевральную полость – возникают плеврит или пневмония, сопровождающиеся расстройствами дыхания;
- в брюшину – наблюдается асцит.
Гипопротеинемия при беременности является одним из признаков позднего гестоза. Как правило, она дополняется:
- чрезмерным увеличением веса;
- отечным синдромом;
- наличием белка в моче;
- гипертензией;
- гипертонусом матки.
Данное состояние расценивается как тяжелое осложнение беременности. Без лечения оно может привести к тромбоцитопении и дистрофии плода.
Что такое отечный синдром и как его лечить?
Отечный синдром — это патологическое состояние, характеризующееся накоплением жидкости в мягких тканях и серозных полостях. Подобное нарушение приводит к появлению ряда негативных процессов. В той или иной степени отечный синдром знаком многим. Легкие отеки могут появляться на протяжении дня и проходить после полноценного отдыха. Однако нередко подобное патологическое состояние свидетельствует о развитии крайне опасных для жизни человека заболеваний.
Степень выраженности напитывания тканей лишней жидкостью может существенно различаться в зависимости от этиологии проблемы. В некоторых случаях этот синдром выражен настолько сильно, что больной утрачивает возможность жить полноценно. К примеру, люди, страдающие от тяжелых форм слоновьей болезни, нередко не могут даже встать с постели, так как увеличение объема жидкости, скапливающейся в нижних и верхних конечностях, становится причиной того, что ими просто невозможно пошевелить.
Лечение
Тактика лечения гипопротеинемии зависит от особенностей состояния пациента. Возможные направления терапии:
- низкий уровень белка в рационе – изменение питания;
- заболевания печени – гепатопротекторы, витамины, глюкоза;
- дисфункции почек – антибиотики, мочегонные средства, противовоспалительные препараты, гемодиализ;
- заболевания ЖКТ – пробиотики, ферменты и так далее.
Помимо лечения основного заболевания, коррекция гипопротеинемии осуществляется с помощью анаболических стероидов – препаратов, которые усиливают синтез белка («Ретаболил»). Для восполнения дефицита белка могут применяться растворы с альбумином – «Лактопротеин», «Аминовен» и другие.
Если гипопротеинемия осложнилась выпотом жидкости в плевру или брюшину, проводят ее аспирацию в ходе лапароцентеза или плевроцентеза соответственно.
Гипопротеинемия
Гипопротеинемия — это патологически обусловленное резкое или постепенное снижение уровня общего белка в составе плазменного компонента крови. Для формирования данного патологического состояния достаточно лишь нарушение алиментарного поступления в организм белковосодержащих продуктов. В этом случае развивается нетяжелая форма гипопротеинемического синдрома. Если же гипопротеинемия развивается как результат сбоя в организме функции печени, которая является главным регулятором белкового обмена, в организме человека возникают тяжелые органические изменения, нуждающиеся в незамедлительной медикаментозной коррекции.
Советуем прочитать: Гипертония с отеком легких
Профилактика
Направления профилактики дефицита белка в крови:
- сбалансированное питание;
- своевременное лечение заболеваний печени, почек и ЖКТ.
С целью предупреждения развития гипопротеинемии необходимы:
- своевременное лечение заболеваний, способствующих ее развитию;
- формирование адекватного рациона с достаточным количеством белка, минеральных веществ, витаминов.
Образование: высшее, 2004 г. (ГОУ ВПО «Курский государственный медицинский университет»), специальность «Лечебное дело», квалификация «Врач». 2008-2012 гг. – аспирант кафедры клинической фармакологии ГБОУ ВПО «КГМУ», кандидат медицинских наук (2013 г., специальность «фармакология, клиническая фармакология»). 2014-2015 гг. – профессиональная переподготовка, специальность «Менеджмент в образовании», ФГБОУ ВПО «КГУ».
Информация является обобщенной и предоставляется в ознакомительных целях. При первых признаках болезни обратитесь к врачу. Самолечение опасно для здоровья!
Лечение гипопротеинемии
Алиментарный тип гипопротеинемии является самым благоприятным в отношении прогноза для выздоровления пациента, так как лечебные мероприятия при данном состоянии ограничиваются коррекцией пищевого поведения пациента. Тяжелые варианты течения гипопротеинемии нуждаются в экстренной медикаментозной коррекции в условиях стационара.
Единственным эффективным методом устранения гипопротеинемии является назначение лекарственных средств, группы анаболических стероидов, действие которых обуславливает усиление продукции белка (внутримышечное введение Ретаболила в дозе 5 мг 1 раз в три недели). Для улучшения эффективности анаболических стероидов данную терапию следует дополнять назначением витаминсодержащих препаратов комплексного действия.
При имеющихся признаках экссудативного плеврита или асцита в качестве симптоматической терапии применяется лапароцентез и плевроцентез.
Гипопротеинемия – какой врач поможет ? При наличии или подозрении на развитие гипопротеинемии следует незамедлительно обратиться за консультацией к таким врачам как гематолог, нефролог и трансфузиолог.
источник
Классификация
Низкое содержание белка может наблюдаться и у здоровых людей (физиологическая гипопротеинемия), например, у детей в возрасте до 3 месяцев или женщин в III триместре беременности. Также концентрация общего белка может оказаться сниженной при длительной госпитализации у лежачих больных. По происхождению патологические гипопротеинемии разделяют на:
1. Гемодилюционные (ложные). Уменьшение уровня белка происходит за счет его «разбавления» избытком жидкой части крови (гиперволемия) при водной интоксикации, олиго- или анурии, первичном гиперальдостеронизме, синдроме неадекватной секреции антидиуретического гормона.
2. Истинные. При данной разновидности гипопротеинемия развивается за счет снижения синтеза белка, повышенных его потерь с мочой либо ускоренного распада. В свою очередь подразделяются на:
- Первичные (наследственные, врожденные). К данной группе относятся различные генетические дефекты синтеза основных белков крови – аутосомно-рецессивная анальбуминемия, X-сцепленная агаммаглобулинемия (болезнь Брутона), врожденные иммунодефициты.
- Вторичные (приобретенные, симптоматические). Наиболее распространенный вариант гипопротеинемий. Возникают преимущественно при заболеваниях печени, почек и голодании.
По снижению содержания отдельной фракции белков выделяют:
- Гипоальбуминемию. Основная разновидность гипопротеинемии, встречается при многих заболеваниях и патологических состояниях.
- Гипоглобулинемию. Низкое содержание глобулинов ассоциировано с иммунодефицитами.
Причины гипопротеинемии
Состояния здоровья, которые влияют на пищеварение или поглощение и использование белков из пищи, часто являются причиной гипопротеинемии.
Ограничение потребления пищи или соблюдение строгих диет также может привести к дефициту белка в организме.
Недоедание и голодание
Гипопротеинемия может быть связана непосредственно с питанием человека, особенно если человек не ест достаточно калорийной пищи или избегает определенных групп продуктов.
Гипопротеинемия, связанная с диетой, может возникнуть в следующих случаях:
- Если человек имеет недостаточный доход, чтобы купить еду и не потребляет достаточно калорий из белка.
- Во время беременности, так как женщинам нужно гораздо больше белка, чем обычно для развития плода. Те, кто не может взять достаточно калорий из источников белка из-за сильной тошноты и рвоты, имеют высокий риск гипопротеинемии.
- У человека есть расстройство пищевого поведения, такое как анорексия и нервная булимия. Эти состояния часто характеризуются питанием, которая не обеспечивает человека достаточным количествов белка.
- Люди, которые придерживаются строгой диеты, такой как та, которая устраняет почти все источники растительных и животных белков, могут подвергаться риску гипопротеинемии.
Болезни печени
Печень играет ключевую роль в переработке белков в организме.
Если печень не функционирует в полном объеме, организм, возможно, не сможет получить достаточно белка для выполнения своих жизненно важных функций. Это может происходить у людей с различными заболеваниями печени, включая печеночная недостаточность, гепатит А, Б или цирроз печени.
Проблемы с почками
Почки помогают фильтровать отходы из крови в мочу. При правильном функционировании почки позволяют белку оставаться в кровотоке.
Однако, когда почки повреждены или не функционируют в полном объеме, они могут пропускать белок в мочу.
Это может произойти у людей, которые имеют артериальную гипертензию (высокое кровяное давление), диабет и некоторые заболевания почек (диабетическая нефропатия, пиелонефрит, почечная недостаточность и проч.). В результате у человека может возникнуть сочетание гипопротеинемии и протеинурии (белок в моче).
Целиакия
Целиакия — это аутоиммунное заболевание, при котором иммунная система по ошибке атакует клетки организма в тонкой кишке.
Эта реакция происходит, когда человек ест продукты, содержащие глютен, белок, который содержится в пшенице, ржи и ячмене.
Аутоиммунное повреждение тонкой кишки может привести к снижению поглощения многих питательных веществ, включая белка.
Воспалительное заболевание кишечника
Некоторые формы воспалительных заболеваний кишечника (ВЗК) вызывают воспаление в тонкой кишке. Именно здесь организм расщепляет многие необходимые питательные вещества и поглощает их.
Повреждение тонкой кишки может привести к различным дефицитам питательных веществ, включая гипопротеинемию.
Анализ крови может выявить, достаточно ли у человека белка в организме.
Врач может выполнить ряд анализов крови, известных как соотношение общего белка, альбумина и альбумина/глобулина. Альбумин и глобулин — два белка, которые производит печень.
Этот анализ может выявить, являются ли уровни общего белка низкими и находятся ли белки альбумина и глобулина на оптимальном уровне.
Если эти два белка находятся в дисбалансе, это может сигнализировать о медицинской проблеме, например, заболевание печени и почек или аутоиммунных заболеваниях.
Этиология отечного синдрома
Появление этого патологического состояния наблюдается при ряде крайне опасных заболеваний, которые могут в самые короткие сроки стать причиной гибели больного. Характерные проявления отечного синдрома зависят от его этиологии. Оценивая степень выраженности и локализацию насыщения мягких тканей жидкостью, в ряде случаев врачи могут определить особенности имеющихся в организме проблем. В настоящее время выделяется общий и местный отек. Каждый их них имеет свои характеристики. Местный отек развивается, как правило, на фоне нарушения оттока жидкости на отдельном участке или в органе. Общий вариант диагностируется в случае нарушения оттока жидкости во всем теле. Эта форма отека обычно указывает на имеющиеся тяжелые нарушения. В зависимости от этиологического фактора отечный синдром может быть:
- почечным;
- кардиогенным;
- травматическим;
- печеночный;
- портальным;
- лимфостатическим;
- ангионевротическим;
- венозным;
- эндокринным;
- нейрогенным;
- мембраногенным;
- ятрогенным;
- гипопротеинемическим и т.д.
Кардиогенный отек
Часто отеки развиваются именно на фоне проблем сердечно-сосудистой системы. Накопление жидкости в нижних конечностях нередко наблюдается при хронической сердечной недостаточности, а также при постоянно повышенном артериальном давлении. Кроме того, нередко накопление жидкости в мягких тканях ног является результатом нарушения работы венозных клапанов.
Советуем прочитать: Какие болезни вызывают отеки глаз
В этом случае наблюдается расширение кровеносных сосудов из-за застоя. Поврежденные стенки вен становятся проницаемыми, поэтому плазма начинает просачиваться в мягкие ткани, вызывая сильнейшие отеки. Кроме того, подобное нарушение может быть вызвано тромбозом на отдельном участке кровеносного сосуда.
Печеночный отек
Скопление жидкости в брюшной полости, а также отечность лица нередко связано с нарушением работы печени. Асцит нередко указывает на развитие декомпенсированной формы цирроза, в результате которого наблюдается нарушение выработки белков, препятствующих пропотеванию плазмы из кровеносных сосудов.
Лимфостатический отек
Лимфостатические отеки имеют крайне разнообразную природу. Ткани тела могут насыщаться жидкость на фоне таких заболеваний, как рецидивирующая рожа, лимфедема, заражение филяриями, слоновости и травмы конечностей. Проблема в этом случае кроется в обструкции лимфатических путей и нарушении оттока жидкости.
Почечный отек
К нарушению работы почек, способному спровоцировать развитие отека мягких тканей верхних и нижних конечностей и лица, могут привести такие заболевания, как системная красная волчанка, амилоидоз, нефропатия беременных, ревматоидный полиартрит, диабетическая гломерулосклероз, лимфолейкоз и т.д.
Эндокринный отек
К эндокринным вариантам относятся отеки, появляющиеся на фоне микседемы. В эту категорию могут быть включены водянка беременных и жировой отечный синдром.
Ятрогенный отек
Яндрогенные или лекарственные отеки нередко развиваются на фоне длительного лечения большими дозами гормональных препаратов, в том числе женскими половыми гормонами. Белковые отеки могут быть спровоцированы приемом некоторых лекарственных средств. Подобное нарушение может быть вызвано прием противовоспалительных гипотензивных препаратов. В некоторых случаях подобное нарушение может быть вызвано ингибиторами МАО и Мидантана.
Нейрогенный отек
отечный синдром
К патологическим состояниям, часто провоцирующим нейрогенные отеки, относятся болезни Пархона и трофедема Межа. Подобное нарушение может быть вызвано таким патологическим состоянием, как рефлекторная симпатическая дистрофия и повреждение гипоталамуса любой этиологии.
Мембраногенный отек
Мембраногенные отеки развиваются на фоне интоксикации организма, а также вследствие воспалительных и аллергических реакций. Насыщение жидкостью мягких тканей может появиться на фоне неврологических заболеваний, которые сопровождаются параличами.
Гипопротеинемический отек
Гипопротеинемические отеки связаны с неправильным питанием. Нередко подобная проблема наблюдается у девушек, которые так сильно стремятся сбросить вес, что отказываются от пищи, содержащей необходимые для жизнедеятельности организма компоненты, в том числе и от белка. В этом случае жидкость накапливается в областях коленей и ступней, проявляется характерная одутловатость лица.
Голодный или алиментарный отек, сопровождающийся опуханием век и лица, часто наблюдается у стремящихся сбросить вес подростков, так как организм не может справиться с имеющимися нагрузками на фоне нерациональной диеты.
К дополнительным симптомам дефицита относится красный язык, стремительное снижение массы тела и хейлиоз. Безбелковые отеки могут быть результатом злоупотребления алкоголем, но случается это нечасто. Гипопротеинемия и скопление жидкости в мягких тканях могут быть вызваны тяжелыми авитаминозами, заболеваниями кишечника, нарушением синтеза альбумина и поражением поджелудочной железы.
Рекомендуемое количество белка
Соблюдение сбалансированной диеты, включающей продукты с высоким содержанием белка, позволит большинству людей получать необходимый им белок.
Рекомендуемая суточная норма белка составляет 0,8 г на килограмм массы тела в день.
Чтобы подсчитать, сколько белка нужно человеку каждый день, они могут умножить свою массу тела в кг на 0,8.
По крайней мере, 10% ежедневных калорий должны быть из белка. Людям, которые очень активны, беременны или пытаются нарастить мышечную массу, может потребоваться больше, чем эти рекомендуемые количества.
Лечение отечного синдрома
Действия врача направляются на стабилизацию состояния пациента и устранение первопричины проблемы.
Для каждого конкретного заболевания, способного вызвать отек, имеется своя схема лечения.
В то же время врач, как правило, назначает и симптоматическую терапию. В некоторых случаях может быть показан прием мочегонных препаратов. Использовать их можно только по рекомендации специалиста, так как в некоторых случаях подобные средства могут стать причиной ухудшения состояния.
Вне зависимости от причины появления отеков рекомендуется снизить суточную дозу потребления жидкости. В тяжелых случаях нужно выпивать не более 1 л воды в день. В деле лечения отеков немаловажное значение имеет изменение рациона.
При большинстве видов этого патологического состояния рекомендуется сократить суточную дозу потребления соли, а лучше всего полностью исключить этот компонент.
Соль способствует задержке жидкости в мягких тканях. Если отечность связана с недостаточным питанием, требуется специальная диета, включающая в себя не только белок, но и другие необходимые организму вещества. Правильное комплексное лечение первичного заболевания в сочетании с терапией, направленной на устранение из организма лишней жидкости, в большинстве случаев позволяет добиться хороших результатов.
источник
Выбор правильных белков
Белки состоят из аминокислот, которые являются строительными блоками тканей. Тело нуждается в большом количестве различных аминокислот, чтобы выполнить его различные функции.
Животные белки предлагают «полные» белки. Примеры включают мясо, рыбу, яйца и птицу. Соя, растительный белок, также является источником полноценного белка.
Эти продукты содержат все незаменимые аминокислоты, необходимые организму.
Растительные белки
Многие растительные белки, включая орехи, семена и бобы, содержат только некоторые необходимые незаменимые аминокислоты.
Люди, соблюдающие вегетарианскую диету, должны следить за тем, чтобы они получали все необходимые им аминокислоты, ежедневно употребляя разнообразные полезные белковые продукты на растительной основе.
Животные белки
Хотя животные белки содержат все незаменимые аминокислоты в адекватных пропорциях, многие из них могут отрицательно повлиять на здоровье. Например, красное мясо часто содержит большое количество насыщенных жиров и калорий.
Рыба может содержать ртуть или другие загрязнители, поэтому детям или беременным женщинам следует избегать употребление рыб.
В целом, употребление в пищу умеренного количества постного мяса, птицы и рыбы является наиболее эффективным способом потребления разнообразных белков.
Что лучше?
Потребление разнообразных белков из животных и растительных источников обычно является лучшим способом избежать развития гипопротеинемии. Хотя большинство растительных продуктов не являются полноценными белками, они содержат клетчатку, витамины, минералы и антиоксиданты, которые помогают бороться с болезнями.
Вместо того, чтобы сосредоточиться на каком-либо одном типе белка, потребление разнообразной диеты является лучшим способом быть здоровым.
С целью предупреждения развития гипопротеинемии необходимы:
- своевременное лечение заболеваний, способствующих ее развитию;
- формирование адекватного рациона с достаточным количеством белка, минеральных веществ, витаминов.
Особенности протекания у беременных
Гипопротеинемия, развившаяся в период беременности, может являться одним из признаков позднего токсикоза (гестоза). Гестоз – тяжелое состояние, повышающее риск перинатальной смертности приблизительно в 5 раз по сравнению со среднестатистической выборкой здоровых беременных.
Главный диагностический критерий гипопротеинемии – снижение концентрации белка в плазме крови до уровня менее 60 г/л, определяющееся в ходе исследования крови лабораторным путем.
Снижение концентрации общего белка в сыворотке крови также может быть относительным и абсолютным.
Относительная гипопротеинемия, как правило, связана с увеличением объема воды в кровеносном русле и наблюдается при следующих состояниях:
· водной нагрузке («водном отравлении»);
· прекращении отделения мочи (анурии);
· уменьшении диуреза (олигурии);
· внутривенном введении больших количеств раствора глюкозы больным с нарушенной выделительной функцией почек;
· повышенной секреции в кровь антидиуретического гормона гипоталамуса – гормона, способствующего задержке воды в организме.
Абсолютная гипопротеинемия, как правило, связана с гипоальбуминемией. При этом уменьшение концентрации общего белка в сыворотке крови возникает при:
· недостаточном поступлении белка в организм (голодание, недоедание, сужение пищевода, нарушение функции желудочно-кишечного тракта, например, воспалительного характера — энтериты, энтероколиты и др.);
· подавлении биосинтеза белка, сопровождающем хронические воспалительные процессы в печени (гепатиты, циррозы печени, интоксикации, атрофия печени);
· врожденных нарушениях синтеза отдельных белков крови (анальбуминемия, болезнь Вильсона-Коновалова, другие дефектопротеинемии — значительно более редко);
· повышенном распаде белка в организме (злокачественные новообразования, обширные ожоги, гиперфункция щитовидной железы (тиреотоксикоз), состояния после операции, длительная лихорадка, травмы, длительное лечение кортикостероидами);
· повышенной потере белка (нефротический синдром, гломерулонефрит, сахарный диабет, длительный (хронический) понос, кровотечения);
· перемещении белка в «третьи» пространства (асцит, плеврит).
Уменьшение концентрации общего белка в сыворотке крови отмечается и при некоторых физиологических состояниях, например, при длительной физической нагрузке, у женщин в последние месяцы беременности и в период лактации.
На уровень общего белка в сыворотке крови может оказывать влияние прием некоторых лекарственных препаратов. Так, например, кортикотропин, кортикостероиды, мисклерон, бромсульфалеин и клофибрат способствуют повышению концентрации общего белка в сыворотке, а пиразинамид, эстрогены — его снижению.
На степень концентрации общего белка может оказывать влияние и положение тела: при изменении горизонтального положения тела на вертикальное концентрация общего белка повышается приблизительно на 10% в течение 30 минут.
Пережатие сосудов во время взятия крови и «работа рукой» также могут привести к возрастанию концентрации общего белка в сыворотке крови.
При интерпретации результатов определения общего белка сыворотки крови необходимо учитывать значение гематокрита — в ряде случаев это помогает отличить относительное изменение общего белка от абсолютного, а следовательно, правильно поставить диагноз и определиться с тактикой лечения.
ПРИ ГОЛОДАНИИ: После 48 часов голодания может увеличиваться концентрация билирубина в крови. Голодание в течение 72 часов снижает концентрацию глюкозы в крови у здоровых людей до 2,5 ммоль/л, увеличивает концентрацию триглицеридов, свободных жирных кислот без значительных изменений концентрации холестерина. Длительное голодание (2 – 4 недели) также способно влиять на ряд лабораторных показателей. Концентрация общего белка, холестерина, триглицеридов, мочевины, липопротеинов в крови снижается; выведение креатинина и мочевой кислоты почками с мочой повышается. Длительное голодание тесно связано со снижением расхода энергии. Вследствие этого в крови снижается концентрация гормонов щитовидной железы – общего тироксина и еще в большей степени трийодтиронина. Голодание также приводит к увеличению содержания в пробах сыворотки крови кортизола и сульфата дегидроэпиандростерона. Увеличение общего белка в сыворотке крови может быть относительным и абсолютным.
Относительная гиперпротеинемия связана с уменьшением содержания воды в сосудистом русле, к чему могут приводить следующие состояния:
· Гипопротеинемия
· Снижение концентрации общего белка в сыворотке крови также может быть относительным и абсолютным.
Абсолютная гипопротеинемия, как правило, связана с гипоальбуминемией. При этом уменьшение концентрации общего белка в сыворотке крови возникает при:
· недостаточном поступлении белка в организм (голодание, недоедание, сужение пищевода, нарушение функции желудочно-кишечного тракта, например, воспалительного характера — энтериты, энтероколиты и др.);
Сопряженная система представляет собой систему, в которой имеет место чередование простых и кратных связей или по-другому – система, в которой кратные связи находятся друг от друга на расстоянии одной одинарной связи. Такая цепь сопряженных связей называется цепью конъюгации.
Сопряжение – перераспределение (выравнивание) электронной плотности в сопряженной системе, приводящее к стабилизации молекулы.
Сопряжение возможно только в том случае, если все атомы, принимающие участие в этом процессе расположены в одной плоскости, т.е. должно выполняться условие копланарности.
3.2. Замкнутые сопряженные системы. Ароматичность.
Сопряженные системы с замкнутой цепью сопряжения – это арены, гетероциклические соединения и небензоидные ароматические структуры. Простейшие замкнутые сопряженные структуры – арены, родоначальником которых является бензол. Бензол был известен издавна, однако долгое время эго структура была не доказана и только в 1865 А.Кекуле предложил изображать строение молекулы бензола в виде правильного шестиугольника с системой чередующихся двойных и простых связей. Изображать формулу бензола принято таким образом и сейчас.
Все атомы углерода в бензольном цикле находятся в sр2- гибридизации, все связи С–С равны между собой, имеют длину 1,40 А° и занимают как бы промежуточное положение между простой (1,54 А°) и двойной (1,33 А°) связями, При этом каждый атом углерода образует три s- связи (одну связь С–Н и две s-связи С–С), лежащих в одной плоскости , т.е. у каждого атома углерода осталось по одному р-электрону, орбитали которых, за счет двукратного перекрывания друг с другом образуют замкнутую p-электронную систему, которая охватывает все атомы углерода. p-Электронная плотность в такой системе распределена равномерно. Замкнутый секстет электронов представляет собой связь, которая отличается от других типов, и ее часто называют ароматической. Электронное строение молекулы бензола можно описать с помощью теории резонанса, согласно которой молекула бензола рассматривается как резонансный гибрид двух предельных (граничных структур)
Понятие ароматичности возникло более ста лет тому назад. В настоящее время к ароматическим системам относятся любые плоские замкнутые циклы, отвечающие критериям ароматичности.
1. Молекула имеет плоское циклическое строение.
2. Все атомы в цикле в состоянии sp2- гибридизации (следовательно s-скелет плоский и все рz-орбитали параллельны.
3. В молекуле существует делокализованная p-электронная система, содержащая 4n + 2 p-электрона , где n = 0,1,2, – натуральный ряд чисел. Это правило получило название правила Хюккеля, предложено в 1931 на основании метода молекулярных орбиталей).
примеры биологически важных ароматических соединений.
Не нашли то, что искали? Воспользуйтесь поиском:
Симптоматические проявления отечного синдрома
При местном проявлении этого патологического состояния в отдельном органе или участке тела скапливается до 0,5 л воды. Общий синдром развивается, когда в организме объем необходимой жидкости превышает норму на 2-4 л. Обычно наблюдается лишняя жидкость в конечностях. Это сопровождается появлением ряда симптомов, в том числе:
- увеличение ноги или руки в объеме;
- набухание кожи;
- покраснение;
- снижение эластичности.
При пальпации отекшего участка обнаруживается тестообразная консистенция кожных покровов. При надавливании остается характерная ямка, которая быстро исчезает. При ложных отеках, к примеру, образованных на фоне микседемы, конечность пальпируется с явных трудом, а получившаяся ямка сохраняется на протяжении нескольких минут, а иногда и часов. На фоне тяжелых отеков кожа в дальнейшем может приобретать бледную окраску, что связано с передавливанием кровеносных сосудов и нарушением питания тканей кислородом. Кроме того, при неблагоприятном развитии этого синдрома на покровах могут появиться трещины, через которые будет постоянно сочиться жидкость.
При лимфатических отеках кожные покровы становятся плотнее на ощупь. При поднятии ноги выше положения тела скопившаяся жидкость убывает довольно медленно. В тяжелых случаях она не исчезает полностью. В дальнейшем постоянное пребывание в тканях белка, попавшего из лимфатической жидкости, приводит к разрастанию коллагеновых волокон и развитию слоновости.
При гипотиреозе отеки выражены на плечах, лице и голенях. При легком надавливании на тканях ямки не бывает, при этом кожа приобретает желтоватый оттенок, шелушится и становится плотной.
Жировые отеки отличаются появлением тяжелых симметричных отеков на ногах. Как правило, это патологическое состояние у очень полных женщин. При этом накопление лишней жидкости в мягких тканях ног усиливается перед менструацией. Область отеков остается мягкой, и при пальпации сохраняются характерные ямки. Могут выявиться признаки хронического венозного застоя.
Прогноз
Выраженная гипопротеинемия может повлечь за собой неблагоприятные последствия для пациента. Падение уровня альбуминов снижает онкотическое давление плазмы крови, что приводит к пропотеванию жидкости в полости тела (брюшную, плевральную, перикардиальную). Также при низкой концентрации белка повышается уровень холестерина в крови, возникает жировая дистрофия печени и нарушается выработка противоинфекционных белков – иммуноглобулинов, белков системы комплемента. Поэтому обнаружение гипопротеинемии требует обращения к врачу.
Отеки, определение, классификация, патогенез, принципы терапии отеков
Отек – это избыточное накопление жидкости в межклеточном пространстве, в результате нарушения обмена воды между кровью и тканями.
Советуем прочитать: Отек ног после флебита
Скопление жидкости в полостях тела получило название водянка.
Различают водянку брюшной полости – асцит, плевральный гидроторакс; перикардиальный – гидроперикардиум и др.
Жидкость, скапливающаяся в этих полостях, называется транссудатом .
Основные местные факторы развития отеков:
а) повышение гидростатического давления в капиллярах;
б) снижение гидростатического (механического) давления в тканях;
в) снижение онкотического и/или осмотического давления плазмы;
г) увеличение онкотического давления периваскулярной жидкости;
д) увеличение проницаемости капилляров;
В зависимости от того, какой из перечисленных факторов является ведущим в патогенезе отека, их делят на:
— гидростатические (гемодинамические, механические, застойные);
В основу клинической классификации отеков положены два принципа:
В соответствии с этим отеки делят на:
Выделяют две группы причин ведущих к развитию отека:
а) патологические состояния, сопровождающиеся задержкой Nа,:
— применение лекарств (кортикостероиды, нестероидные противовоспалительные препараты)
б) гипопротеинемии – болезни печени, нефротический синдром.
Причины и патогенез гемодинамических отеков.
Развитие этих отеков связано с увеличением гидростатического давления в капиллярах из-за нарушения оттока венозной крови. Первичное увеличение А/Д, как правило, не ведет к возникновению отеков.
Венозный оттек нарушается при целом ряде патологических состояний:
— венозная гиперемия в большом или малом круге кровообращения при недостаточности кровообращения;
— сдавливание вен матки при беременности.
Способствует развитию гемодинамических отеков также снижение тканевого механического сопротивления из-за обеднения тканей колагенном (при воспалении); снижение давления в полостях, например, в плевральной (что может привести к развитию гидроторакса.
Первоначально гемодинамические отеки возникают на ногах, а затем «поднимаются» в верхнюю часть туловища.
Причины гипоонкотических отеков.
При снижении концентрации белка плазмы крови ниже 5% онкотическое давление в ней становится неспособным удерживать воду в просвете капилляра и она начинает выходить в ткани.
К гипоонкии приводят:
б) нарушение белков – синтетической функции печени;
в) значительные потери белка при энтеропатиях, обширных ожогах;
г) белковое и полное голодание.
Иногда данный вид отеков развивается при при нормальном содержании белка, но при выраженной диспротеинемии, когда резко снижен альбумин – глобулиновый коэффициент ( в норме 2:10).
Развитие отека по онкотическому механизму наблюдается при тканевой гиперонкии. Отек в этом случае носит местный характер.
Это происходит при:
— выходе плазменных белков в ткани;
— выходе клеточных белков при их альтерации
— повышении гидрофильности белков в межклеточном пространстве под влиянием ионов H,Nа, гистомина, серотоина, тироксина, при дефиците Са.
Патогенез мемброгенных отеков.
Мембраногенные отеки связаны с повышенной проницаемостью стенки сосудов. К повышению проницаемости сосудистой стенки приводят различные нейрогенные механизмы, яды, ацидоз, повышение температуры, а также биологически активные вещества — гистамин, брадикинин, серотонин.
Множество этих причин, повышающих проницаемость капилляров, предполагает участие мембранного фактора в развитии самых различных отеков, но ведущим он является для воспалительного, аллергического, токсического и ангионевротического отеков. Повышение проницаемости сосудистой стенки ведет в данном случае к выходу большого количества альбуминов в межклеточную жидкость ,а альбумины эффективно связывают и удерживают жидкость в тканях.
Механизмы развития лимфогенных отеков.
Лимфогенный отек обусловлен нарушением отека лимфы, что ведет к накоплению в тканях отечной жидкости богатой белком.
Причинами затрудненного оттока лимфы могут быть врожденная гипоплазия лимфотических сосудов, сдавление их рубцами или сдавление опухолями и метастазами.
Длительный лимфатический отек ведет к накоплению в ткани белка с последующим разрастанием коллагановых волокон и деформацией органа – слоновостью.
Патогенез сердечных отеков.
Механизм развития сердечных отеков можно представить в виде схемы:
Снижение сократительной способности миокарда
Снижение ОЦЖ и венозный застой.
| оттока крови по венозной системе. | снижение почечного кровотока | Раздражение волюморецепторов правого предсердия | Гипоксия тканей. |
| Активация Ренин – ангиотензин- альдостеронового механизма. | Ацидоз | ||
| Увеличение реабсорбцииNа | Увеличение проницаемости местных сосудов. | ||
| Увеличение Р осм. | |||
| Увеличение выработки АДГ | |||
| Задержка воды |
Нефротический отек связан с массивной почечной протеинурией, развитием гипопротеинемии, гипоонкии и переходом значительного количества жидкости в ткани. Формирующаяся при этом гиповолемия и снижение ОЦК включает ренин- ангиотезин – альдостероновый механизм задержки Nа, к этому подключается АДГ-механизм задержки воды.
Патогенез почечных (нефротических) отеков.
Подобная двойственность механизмов: гипоонкия с одной стороны и задержка H2О почками с другой, делает нефротические отеки весьма выраженными и стойкими.
Патогенез нефритических отеков.
Нефритические отеки возникают при заболеваниях почек с преимущественным диффузным поражением клубочкового аппарата воспалительного и/или аллергического происхождения в корковом слое почек обуславливает усиление секреции ренина юкстагломерулярными (ЮГА) клетками, что, в свою очередь, активирует систему ренин – ангиотензин – II- альдостерон – АДГ.
Это ведет к эадержке в организме Nа и воды. Важно, что для диффузного гломерулонефрита характкрно повреждение мембран микрососудов и, прежде всего, каппиляров во многих тканях и органах организма. Повышение их проницаемости является важным механизмом развития нефритических отеков. Постепенное поражение почек при гломерулонефрите ведет к такому же постепенному нарастанию отеков.
Впрочем, первоначально жидкость начинает выходить из сосудов, расположенных в рыхлых тканях. Поэтому раньше всего нефротические отеки возникают в сетчатке глаз, в области век, в мягких тканях лица, шеи, а затем и туловища.
Патогенез печеночных отеков.
В возникновении печеночных отеков главная роль отводится повреждению печеночной паренхимы при гепатитах и циррозе печени.
При этом безусловная роль принадлежит следующим механизмам:
а) – поврежденные гепотациты не синтезируют достаточного количества альбуминов, снижение концентрации которых в крови включает гипоонкотический путь перехода жидкости в ткани;
б) – развивающаяся при циррозе печени соединительная ткань, сдавливая кровеносные сосуды, является причиной портального застоя, что затрудняет отток крови от органов брюшной полости, приводя к формированию асцита;
в) – снижение ОЦЖ, вследствие задержки ее печенью приводит с одной стороны к снижению активности волюморецепторов левого предсердия и увеличению выброса АДГ, а с другой стороны – к раздражению волюморецепторов правого предсердия и повышению секреции альдостерона;
г) – печень с нарушенным кровотоком (застойная) плохо инактивирует гормоны, в том числе альдостерон и АДГ, которые способствует задержке солей и воды в организме.
Коррекция
Для борьбы с гиперпротеинемией необходимо лечение основного заболевания, на фоне которого она развилась. Физиологическая гиперпротеинемия не требует никакого вмешательства, так как не является признаком болезни или патологического состояния. Для коррекции гемоконцентрационной гиперпротеинемии достаточно устранить дефицит жидкости перорально либо внутривенным введением кристаллоидных растворов. В остальных случаях проводится следующие мероприятия:
- Противоинфекционная терапия. Для элиминации инфекционного возбудителя назначаются антибактериальные (амоксициллин, левофлоксацин), антипаразитарные (гидроксихлорохин, мефлохин). При генерализованных бактериальных инфекциях (сепсис, эндокардит) рекомендуется комбинация минимум из 2-х антибиотиков разных групп.
- Противовоспалительная терапия. С целью купирования воспалительного процесса и достижения ремиссии аутоиммунных заболеваний применяются глюкокортикостероиды (преднизолон), иммуносупрессанты (циклофосфамид, азатиоприн), производные 5-аминосалициловой кислоты (сульфасалазин). При тяжелом течении прибегают к генно-инженерным биологическим препаратам (моноклональным антителам), таким как ритуксимаб.
- Химиотерапия. В случае подтверждения монокональной гаммапатии для замедления пролиферации опухолевых клеток используются комбинации химиотерапевтических средств – аналогов нуклеозидов (флударабин), алкилирующих препаратов (хорамбуцил), ингибиторов фактора некроза опухоли.
- Пересадка костного мозга. Некоторой группе пациентов с онкогематологическими заболеваниями совместно с курсами химиотерапии показана трансплантация гемопоэтических клеток.
- Плазмаферез. Плазмаферез – единственный способ прямого снижения уровня белка в сыворотке крови. Удаление из организма больного избытков белка назначается только при миеломной болезни и макроглобулинемии Вальденстрема, сопровождающихся крайне высокой гиперпротеинемией, вызывающей ярко выраженную картину СГВ.
Гиперпротеинемия в подавляющем большинстве случаев не несет никаких неблагоприятных последствий для пациента. Прогноз определяется тем заболеванием, которое послужило причиной развития этого лабораторного феномена. Исключением являются высокие показатели белка при моноклональных гаммапатиях, когда гиперпротеинемия может стать причиной коматозного состояния, трофических язв и гангрены конечностей, хронической почечной недостаточности. Поэтому любое превышение референсных значений белка, особенно высокое и стойкое, требует обращения к врачу.
| МКБ-9 | MeSH | DiseasesDB | MedlinePlus |